OPASNOST PO ZDRAVLJE LJUDI
3.1.1. Definicija
3.1.1.1. Akutna toksičnost predstavlja one štetne efekte koji se javljaju posle peroralne ili dermalne primene pojedinačne doze supstance ili smeše, odnosno unošenja više doza tokom 24 sata ili inhalacionog izlaganja u trajanju od četiri sata.
3.1.1.2. Klasa opasnosti akutna toksičnost se deli na:
- akutnu peroralnu toksičnost,
- akutnu dermalnu toksičnost,
- akutnu inhalacionu toksičnost.
3.1.2. Kriterijumi za klasifikaciju supstanci kao akutno toksičnih
3.1.2.1. Supstance mogu biti klasifikovane u jednu od četiri kategorije akutne toksičnosti na osnovu puta izlaganja koji može biti peroralni, dermalni ili inhalacioni u skladu sa numeričkim kriterijumima koji su prikazani u Tabeli 3.1.1. koja je data u ovom prilogu. Vrednosti za akutnu toksičnost su prikazane kao (približne) LD50 (peroralna, dermalna) ili LC50 (inhalaciona) vrednosti ili kao procenjena vrednost akutne toksičnosti (Acute toxicity estimates - ATE).
Napomene su date ispod Tabele 3.1.1.
Tabela 3.1.1. Kategorije akutne toksičnosti i procenjene vrednosti akutne toksičnosti (ATE) za odgovarajuće kategorije
Put izlaganja |
Kategorija 1 |
Kategorija 2 |
Kategorija 3 |
Kategorija 4 |
Peroralno (mg/kg telesne mase) |
ATE ≤ 5 |
5 < ATE ≤ 50 |
50 < ATE ≤ 300 |
300 < ATE ≤ 2000 |
Dermalno (mg/kg telesne mase) |
ATE ≤ 50 |
50 < ATE ≤ 200 |
200 < ATE ≤ 1000 |
1000 < ATE ≤ 2000 |
Gasovi (ppmV)* |
ATE ≤ 100 |
100 < ATE ≤ 500 |
500 < ATE ≤ 2500 |
2500 < ATE ≤ 20000 |
Pare (mg/l) |
ATE ≤ 0,5 |
0,5 < ATE ≤ 2,0 |
2,0 < ATE ≤ 10,0 |
10,0 < ATE ≤ 20,0 |
Prašina i magla (mg/l) |
ATE ≤ 0,05 |
0,05 < ATE ≤ 0,5 |
0,5 < ATE ≤ 1,0 |
1,0 < ATE ≤ 5,0 |
Napomena (*): Koncentracije gasa su izražene u ppmV (parts per million per volume). |
||||
Napomene:
1) Procenjena vrednost akutne toksičnosti (ATE) za klasifikaciju supstance izvodi se na osnovu LD50/LC50 vrednosti, kada su dostupne.
2) Procenjena vrednost akutne toksičnosti (ATE) za klasifikaciju supstance u smeši izvodi se na osnovu sledećih parametara:
- LD50/LC50 vrednosti, kada su dostupne,
- odgovarajućih konvertovanih vrednosti iz Tabele 3.1.2. koja je data u ovom prilogu, a koje se odnose na rezultate ispitivanja akutne toksičnosti, ili
- odgovarajućih konvertovanih vrednosti iz Tabele 3.1.2. koja je data u ovom prilogu, a koje se odnose na klasifikacionu kategoriju.
3) Opšte granične koncentracije za inhalacionu toksičnost u tabeli zasnivaju se na rezultatima četvoročasovnog izlaganja supstanci u uslovima ispitivanja. Konverzija vrednosti koje su dobijene posle jednočasovnog izlaganja može se dobiti deljenjem faktorom 2 za gasove i pare i faktorom 4 za prašinu i maglu.
4) Za pojedine supstance atmosfera u kojoj se vrši ispitivanje nije samo u obliku pare već predstavlja mešavinu tečne i gasovite faze. Za druge supstance atmosfera se može sastojati od pare koja je na granici gasne faze. U ovom drugom slučaju, klasifikacija se zasniva na ppmV vrednostima i to na sledeći način: kategorija 1 (100 ppmV), kategorija 2 (500 ppmV), kategorija 3 (2500 ppmV), kategorija 4 (20000 ppmV).
3.1.2.1.1. Pojmovi: "prašina", "magla" i "para" u smislu ovog pravilnika imaju sledeće značenje:
- Prašina jesu čvrste čestice supstance ili smeše suspendovane u gasu (obično vazduh);
- Magla jesu tečne čestice supstance ili smeše suspendovane u gasu (obično vazduh);
- Para jeste gasoviti oblik supstance ili smeše oslobođen iz njenog tečnog ili čvrstog stanja.
Prašina se obično formira mehaničkim putem. Magla najčešće nastaje kondenzovanjem prezasićenih para ili fizičkim raspršivanjem tečnosti. Čestice prašine i magle su veličine od manje od 1 μm do oko 100 μm.
3.1.2.2. Posebne napomene za klasifikaciju supstanci kao akutno toksičnih
3.1.2.2.1. Ispitivanja za procenu akutne toksičnosti supstanci unetih peroralno ili inhalacijom obično se vrše na pacovima, dok se dermalna akutna toksičnost supstanci ispituje na kunićima ili pacovima. Kada su dostupni podaci o akutnoj toksičnosti neke supstance na različitim vrstama životinja, odgovarajuća LD50 vrednost biće izabrana na osnovu naučne procene između više validnih i dobro sprovedenih ispitivanja.
3.1.2.3. Posebne napomene za klasifikaciju supstanci kao akutno toksičnih koje se unose inhalacijom
3.1.2.3.1. Jedinice u kojima se izražava inhalaciona toksičnost zavise od oblika inhaliranog materijala. Vrednosti za prašinu i maglu izražavaju se u mg/l. Vrednosti za gasove izražavaju se u ppmV. S obzirom na poteškoće koje postoje u ispitivanju para, od kojih se neke sastoje od tečne i gasne faze, vrednosti u tabeli su date u jedinicama mg/l. Ipak, za pare koje su skoro sasvim u gasovitom stanju, klasifikacija se zasniva na vrednostima u ppmV.
3.1.2.3.2. Od naročitog značaja za klasifikaciju u odnosu na inhalacionu toksičnost je korišćenje dobro određenih vrednosti za kategorije visoke toksičnosti za prašinu i maglu. Inhalirane čestice prosečnog aerodinamičkog prečnika (Mass Median Aerodynamic Diameter - MMAD) između 1 i 4 mikrona taložiće se u svim delovima respiratornog trakta pacova. Ovaj opseg veličine čestica odgovara maksimumu doze od oko 2 mg/l. Da bi se rezultati eksperimenata na životinjama mogli primeniti na izloženost ljudi, idealno je prašinu i maglu ispitivati na pacovima u ovom opsegu.
3.1.2.3.3. Dodatne napomene u vezi klasifikacije za inhalacionu toksičnost: ukoliko postoje podaci koji ukazuju da se mehanizam toksičnosti zasniva na korozivnosti, supstanca ili smeša obeležavaju se i kao korozivna za respiratorne organe (videti napomenu 1 u odeljku 3.1.4.1. ovog priloga). Korozija respiratornih organa je razaranje tkiva respiratornih organa nakon jednokratnog, ograničenog perioda izlaganja koje je analogno korozivnom oštećenju kože i obuhvata i razaranje sluzokože. Procena korozivnog delovanja može biti zasnovana na stručnoj proceni korišćenjem podataka kao što su: iskustvo o delovanju na ljude i životinje, postojeći podaci dobijeni in vitro ispitivanjem, podaci o pH vrednostima, podaci o sličnim supstancama i drugi prikladni podaci.
3.1.3. Kriterijumi za klasifikaciju smeša kao akutno toksičnih
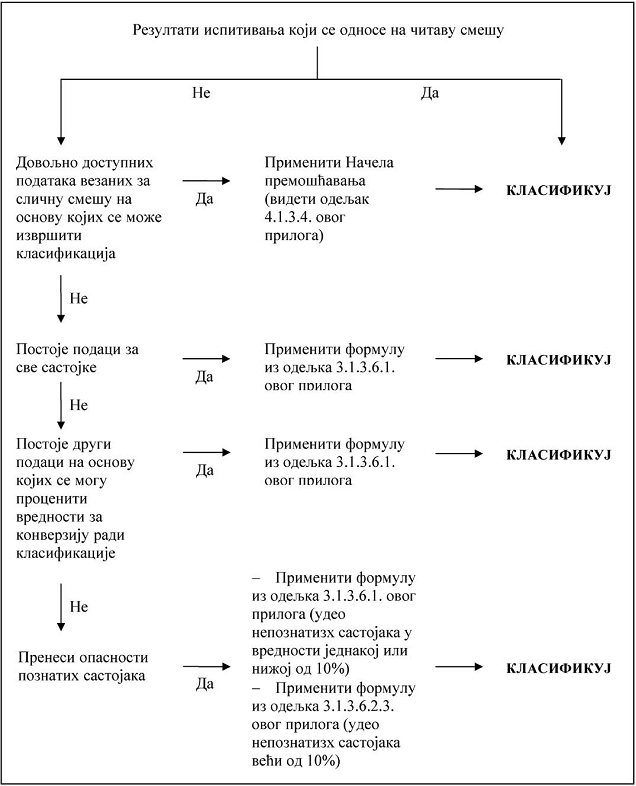
3.1.3.1. Kriterijumi za klasifikaciju supstanci kao akutno toksičnih dati su u odeljku 3.1.2. ovog priloga i zasnivaju se na podacima o letalnim dozama (koji su dobijeni ispitivanjem ili proračunom). Kod smeša je neophodno pribaviti ili proračunati podatke koje omogućavaju klasifikaciju smeša. Pristup klasifikaciji u odnosu na akutnu toksičnost je višestepen i zavisi od broja dostupnih podataka o smeši i njenim sastojcima. Šematski prikaz procedura koje se primenjuju dat je na slici 3.1.1. koja je data u ovom prilogu.
3.1.3.2. Pri klasifikaciji smeša u odnosu na akutnu toksičnost, razmatra se svaki put izlaganja, ali su dovoljni podaci (procenjeni ili dobijeni ispitivanjima) za samo jedan put izlaganja ako postoje za sve sastojke i da nema pouzdanih podataka koji ukazuju na akutnu toksičnost za više puteva izlaganja. Kada postoje pouzdani podaci o toksičnosti za više puteva izlaganja, klasifikacija se vrši za sve relevantne puteve izlaganja. Razmatraju se svi dostupni podaci. Piktogram opasnosti i reč upozorenja ukazuju na kategoriju opasnosti sa najvećim stepenom opasnosti i navode se sva relevantna obaveštenja o opasnosti.
3.1.3.3. Da bi se iskoristili svi dostupni podaci o nekoj smeši radi njene klasifikacije prema stepenu opasnosti, date su određene pretpostavke koje se primenjuju kada je potrebno, u višestepenom pristupu:
1) "relevantni sastojci" smeše su oni koji su u njoj sadržani u koncentraciji od 1% (m/m za čvrste materije, tečnosti, prašinu, maglu i pare i V/V za gasove) ili većoj, osim ukoliko postoji razlog da se neki sastojak prisutan u smeši u koncentraciji manjoj od 1% uzme kao relevantan za njenu klasifikaciju u odnosu na akutnu toksičnost (videti Tabelu 1.1);
2) kada se već klasifikovana smeša koristi kao sastojak druge smeše, mogu se koristiti stvarne ili izvedene vrednosti akutne toksičnosti (ATE) određene za ovu smešu, a klasifikacija nove smeše vrši se na osnovu formula koje su date u odeljcima 3.1.3.6.1. i 3.1.3.6.2.3. ovog priloga;
3) ako su konvertovane procenjene vrednosti akutne toksičnosti za sve sastojke smeše u istoj kategoriji opasnosti, onda se smeša klasifikuje u tu kategoriju;
4) kada su za sastojke smeše dostupni samo opsezi vrednosti za akutnu toksičnost (ili podaci o kategoriji opasnosti akutne toksičnosti), oni se radi izračunavanja klasifikacije nove smeše primenom formule date u odeljcima 3.1.3.6.1. i 3.1.3.6.2.3. ovog priloga mogu konvertovati u procenjene vrednosti u skladu sa Tabelom 3.1.2. koja je data u ovom odeljku.
Slika 3.1.1. Višestepeni pristup za klasifikaciju smeša u odnosu na akutnu toksičnost

3.1.3.4.Klasifikacija smeša kada su dostupni podaci o akutnoj toksičnosti za samu smešu
3.1.3.4.1. Kada je sama smeša ispitana sa ciljem da se utvrdi njena akutna toksičnost, klasifikacija se vrši na osnovu istih kriterijuma kao i za supstance, što je objašnjeno u Tabeli 3.1.1. ovog priloga. Ukoliko rezultati ispitivanja koji se odnose na samu smešu nisu poznati, primenjuje se procedura iz odeljaka 3.1.3.5 i 3.1.3.6. ovog priloga.
3.1.3.5. Klasifikacija smeša kada nisu dostupni podaci o akutnoj toksičnosti za samu smešu: Načela premošćavanja
3.1.3.5.1. Kada sama smeša nije ispitana radi utvrđivanja njene akutne toksičnosti, ali postoji dovoljno podataka koji se odnose na pojedinačne sastojke i slične ispitane smeše tako da se stepen njene potencijalne opasnosti može odrediti, ovi podaci se koristite na osnovu načela premošćavanja iz odeljka 1.1.3. ovog priloga.
3.1.3.5.2. Ako je ispitana smeša razblažena rastvaračem koji je klasifikovan u istu ili nižu klasu opasnosti za toksičnost u odnosu na najmanje toksičan prvobitni sastojak i ako se ne očekuje da rastvarač utiče na toksičnost drugih sastojaka, onda se nova smeša može klasifikovati kao i početna ispitana smeša. Druga mogućnost je primena formule koja je data u odeljku 3.1.3.6.1 ovog priloga.
3.1.3.6. Klasifikacija smeša na osnovu sastojaka smeše (formula aditivnosti)
3.1.3.6.1. Klasifikacija smeša kada su poznati podaci za sve sastojke
Kako bi se osigurala odgovarajuća klasifikacija i da bi se proračuni vršili samo jednom za sve sisteme, sektore i kategorije, procenjena akutna toksičnost (ATE) sastojaka se razmatra na sledeći način:
1) uključiti sastojke sa poznatom akutnom toksičnošću koji pripadaju jednoj od kategorija akutne toksičnosti datih u Tabeli 3.1.1.,
2) zanemariti sastojke za koje se smatra da nisu akutno toksični (npr. voda, šećer),
3) zanemariti sastojke ukoliko su dostupni podaci dobijeni ispitivanjem granične doze (na gornjoj granici za kategoriju 4, za odgovarajući put izlaganja kao što je navedeno u Tabeli 3.1.1. koja je data u ovom prilogu) i ne pokazuju akutnu toksičnost.
Sastojci koji se razmatraju u okviru ovog odeljka su sastojci čija je procenjena akutna toksičnost (ATE) poznata. Za odgovarajuću primenu dostupnih podataka u formulama koje su date u ovom odeljku i u odeljku 3.1.3.6.2.3. ovog priloga videti napomenu 2) ispod Tabele 3.1.1. i odeljak 3.1.3.3. ovog priloga.
Procenjena akutna toksičnost (ATE) za smešu određuje se proračunom na osnovu ATE vrednosti za sve relevantne sastojke za peroralnu, dermalnu i inhalacionu toksičnost prema sledećoj formuli:
![]()
pri čemu je:
Ci - koncentracija sastojka i (% m/m ili % V/V);
i - pojedinačni sastojak od 1 do n;
n - broj sastojaka;
ATEi - procenjena akutna toksičnost za sastojak i.
3.1.3.6.2. Klasifikacija smeša kada nisu poznati podaci za sve sastojke
3.1.3.6.2.1. Kada procenjena akutna toksičnost (ATE) nije poznata za neki od pojedinačnih sastojaka smeše, ali podaci koji o tom sastojku postoje mogu da posluže da se konverzijom izvede takva vrednost kao što je prikazano u Tabeli 3.1.2. koja je data u ovom prilogu, primenjuje se formula data u odeljku 3.1.3.6.1. ovog priloga. Ovo podrazumeva sledeće:
1) ekstrapolaciju između peroralne, dermalne i inhalacione procenjene akutne toksičnosti(13). Ovakva procena može zahtevati odgovarajuće farmakodinamičke i farmakokinetičke podatke;
2) podatke dobijene na osnovu iskustva o izlaganju ljudi koji potvrđuju toksične efekte, ali bez podataka o letalnim dozama;
3) podatke o akutnim toksičnim efektima supstance dobijene u drugim ispitivanjima, ali koji ne pružaju podatke o letalnim dozama ili
4) podatke o srodnim supstancama dobijene na osnovu odnosa strukture i aktivnosti.
Za ovaj pristup klasifikaciji uglavnom su potrebni dodatni tehnički podaci, kao i dobro obučen i iskusan stručnjak (stručna procena, videti odeljak 1.1.1. ovog priloga) koji će izvršiti pouzdanu procenu akutne toksičnosti. Ukoliko ovi podaci nisu dostupni treba primeniti odredbe iz odeljka 3.1.3.6.2.3. ovog priloga.
3.1.3.6.2.2. U slučaju kada je u smeši, u količini od 1% ili većoj, upotrebljen neki sastojak za koji ne postoji nijedan odgovarajući podatak, ne može se proceniti akutna toksičnost te smeše. U tom slučaju smeša se klasifikuje samo na osnovu poznatih podataka o sastojcima i dodaje se obaveštenje da se "x" procenata smeše sastoji od sastojka nepoznate toksičnosti.
3.1.3.6.2.3. Ukoliko je ukupna koncentracija sastojka nepoznate akutne toksičnosti u smeši 10% ili manja, primenjuje se formula iz odeljka 3.1.3.6.1. ovog priloga. Ukoliko je ukupna koncentracija ovakvih sastojaka veća od 10% primenjuje se formula iz odeljka 3.1.3.6.1. ovog priloga ali sa korekcijama, tako da odgovara ukupnom procentu nepoznatih sastojaka:
![]()
Tabela 3.1.2. Konverzija eksperimentalno dobijenih opsega vrednosti akutne toksičnosti (ili kategorije opasnosti akutne toksičnosti) u procenjenu vrednost akutne toksičnosti za primenu u formulama koje se koriste za klasifikaciju smeša
Put izlaganja |
Klasifikaciona kategorija ili eksperimentalno |
Konvertovana akutna toksičnost |
Peroralno |
0 < kategorija 1 ≤ 5 |
0,5 |
Dermalno |
0 < kategorija 1 ≤ 50 |
5 |
Gasovi |
0 < kategorija 1 ≤ 100 |
10 |
Pare |
0 < kategorija 1 ≤ 0.5 |
0,05 |
Prašina/magla |
0 < kategorija 1 ≤ 0,05 |
0,005 |
Napomena 1: Ove vrednosti se koriste u izračunavanju ATE (procenjene vrednosti akutne toksičnosti) za klasifikaciju smeša na osnovu njihovih sastojaka i ne predstavljaju rezultate ispitivanja.
__________
(13) Kada smeše sadrže sastojke za koje nema podataka o akutnoj toksičnosti za svaki put izlaganja, vrednosti procenjene akutne toksičnosti mogu se dobiti ekstrapolacijom dostupnih podataka i primeniti na relevantne puteve izlaganja (videti odeljak 3.1.3.2. ovog priloga). Međutim, ispitivanje za određeni put izlaganja može da se zahteva drugim propisom. U tom slučaju, klasifikacija za taj put izlaganja vrši se u skladu sa tim propisom.
3.1.4. Elementi obeležavanja
3.1.4.1. Elementi obeležavanja za supstance i smeše koje ispunjavaju uslove da budu klasifikovane u ovu klasu opasnosti dati su u Tabeli 3.1.3. koja je data u ovom prilogu.
Tabela 3.1.3. Elementi obeležavanja za akutnu toksičnost
Klasifikacija |
Kategorija 1 |
Kategorija 2 |
Kategorija 3 |
Kategorija 4 |
GHS piktogram opasnosti |
|
|
|
|
Reč upozorenja |
Opasnost |
Opasnost |
Opasnost |
Pažnja |
Obaveštenje o opasnosti: |
H300: |
H300: |
H301: |
H302: |
- Dermalno |
H310: |
H310: |
H311: |
H312: |
- Inhalaciono |
H330: |
H330: |
H331: |
H332: |
Obaveštenja o merama predostrožnosti |
P264 |
P264 |
P264 |
P264 |
Obaveštenja o merama predostrožnosti |
P301+P310 |
P301+P310 |
P301+P310 |
P301+P312 |
Obaveštenja o merama predostrožnosti |
P405 |
P405 |
P405 |
|
Obaveštenja o merama predostrožnosti |
P501 |
P501 |
P501 |
P501 |
Obaveštenja o merama predostrožnosti |
P262 |
P262 |
P280 |
P280 |
Obaveštenja o merama predostrožnosti |
P302+P350 |
P302+P350 |
P302+P352 |
P302+P352 |
Obaveštenja o merama predostrožnosti |
P405 |
P405 |
P405 |
|
Obaveštenja o merama predostrožnosti |
P501 |
P501 |
P501 |
P501 |
Obaveštenja o merama predostrožnosti |
P260 |
P260 |
P261 |
P261 |
Obaveštenja o merama predostrožnosti |
P304+P340 |
P304+P340 |
P304+P340 |
P304+P340 |
Obaveštenja o merama predostrožnosti |
P403+P233 |
P403+P233 |
P403+P233 |
|
Obaveštenja o merama predostrožnosti |
P501 |
P501 |
P501 |
|
Napomena 1: Pored toga što je klasifikovana kao inhalaciono toksična, ukoliko postoje podaci koji ukazuju na to da se mehanizam toksičnosti zasniva na korozivnosti, na etiketi uz takvu supstancu ili smešu treba da stoji i oznaka: EUH071: "korozivno za respiratorne organe", videti odeljak 3.1.2.3.3. ovog priloga. To znači da pored piktograma opasnosti koji ukazuje na akutnu toksičnost treba da stoji i piktogram opasnosti koji ukazuje na korozivno oštećenje (koristi se za korozivno dejstvo na oko ili kožu), kao i obaveštenje o opasnosti: "korozivna supstanca" ili "korozivno za respiratorne organe".
Napomena 2: U slučaju kada je u smeši u količini od 1% ili većoj upotrebljen neki sastojak za koji ne postoji nijedan odgovarajući podatak, na etiketi se navodi dodatno obaveštenje da "smeša sadrži x% sastojka nepoznate toksičnosti" (videti odeljak 3.1.3.6.2.2. ovog priloga).
3.2. Korozivno oštećenje/iritacija kože
3.2.1. Definicije
Korozivno oštećenje kože jeste nastanak ireverzibilnih oštećenja kože, odnosno vidljive nekroze u epidermisu ili dermisu, nakon četvoročasovne primene ispitivane supstance. Korozivna oštećenja kože se karakterišu prema tipu izazvanog oštećenja kao: ulkusi, krvarenja, krvave kraste i na kraju perioda posmatranja od 14 dana prema promeni boje kože uslovljene perutanjem i pojavi područja sa alopecijom i ožiljcima. U cilju procene nejasnih oštećenja potrebno je razmotriti histopatologiju.
Iritacija kože predstavlja nastanak reverzibilnih oštećenja kože koja prate primenu ispitivane supstance tokom četiri sata.
3.2.2. Kriterijumi za klasifikaciju supstanci
3.2.2.1. Pre nego što se pristupi ispitivanju, neophodno je razmotriti nekoliko faktora koji određuju korozivni i iritativni potencijal supstance. Čvrste supstance (prah) mogu da postanu korozivne ili iritativne kada se navlaže ili kada dođu u kontakt sa vlažnom kožom ili mukoznim membranama. Iskustva kod ljudi i podaci dobijeni na životinjama koji se odnose na jednokratno ili višekratno izlaganje, predstavljaju prvi nivo analize, pošto direktno obezbeđuju relevantne podatke o uticaju ovih supstanci na kožu (videti član 5. ovog pravilnika). U nekim slučajevima, pri klasifikaciji, mogu se koristiti i dostupni podaci koje se odnose na strukturno slične supstance.
3.2.2.2. I pored izvesnih odstupanja, ekstremne pH vrednosti kao što su ≤ 2 i ≥ 11,5 mogu ukazati na potencijal da se prouzrokuju efekti na koži, pogotovo kada je poznat puferni kapacitet. Za ovakve supstance se očekuje da mogu imati značajan efekat na kožu. Ukoliko razmatranja alkalne/kisele rezerve ukazuju na to da supstanca najverovatnije nema korozivna svojstva uprkos niskoj ili visokoj pH vrednosti, sprovode se dodatna ispitivanja, primenom odgovarajućeg validiranog in vitro testa, kojima bi se ova pretpostavka potvrdila.
3.2.2.3. Ukoliko je supstanca visoko toksična kada se unese preko kože, ne preporučuje se ispitivanje njenog iritativnog/korozivnog delovanja na kožu jer količina supstance koja se primenjuje u ispitivanjima prevazilazi toksičnu dozu i kao posledicu ima uginuće laboratorijskih životinja. Kada se u okviru ispitivanja akutne toksičnosti posmatra i iritativno/korozivno dejstvo na kožu i ukoliko je ovaj efekat prisutan primenom granične doze, ne sprovode se dodatna ispitivanja, ako su razblaženja i vrste na kojima je ispitivanje sprovedeno odgovarajući.
3.2.2.4. Sve gore navedene dostupne podatke o supstanci ili smeši treba razmotriti prilikom donošenja odluke o potrebi izvođenja in vivo ispitivanja iritacije kože.
Iako se ovakvi podaci mogu dobiti na osnovu procene pojedinačnih parametara u okviru višestepenog pristupa (videti odeljak 3.2.2.5. ovog priloga), npr. baze alkalnih metala sa ekstremnim pH vrednostima treba posmatrati kao supstance korozivne za kožu, prednost ima razmatranje svih postojećih podataka i utvrđivanje kvaliteta podataka, što je značajno kada su podaci dostupni samo za neke, ali ne i za sve parametre. Ako je neophodna procena svakog pojedinačnog parametra, prednost imaju podaci dobijeni pri izlaganju ljudi, zatim podaci dobijeni pri izlaganju životinja i rezultati ispitivanja sprovedenih na životinjama i na kraju drugi izvori podataka.
3.2.2.5. Pri proceni inicijalnih podataka primenjuje se višestepeni pristup, tamo gde je prikladan, imajući u vidu da u određenim slučajevima ne odgovaraju svi elementi ovog pristupa.
3.2.2.6. Korozivno oštećenje
3.2.2.6.1. Na osnovu rezultata ispitivanja na životinjama supstanca se klasifikuje kao korozivna, kao što je dato u Tabeli 3.2.1. koja je data u ovom prilogu. Korozivna supstanca je supstanca koja dovodi do oštećenja tkiva kože, odnosno vidljive nekroze u epidermisu ili dermisu kod najmanje jedne od tri ispitivane životinje nakon izlaganja u trajanju od četiri sata. Korozivna oštećenja se karakterišu prema tipu izazvanog oštećenja kao: ulkusi, krvarenje, krvave kraste i na kraju perioda posmatranja od 14 dana prema promeni boje kože uslovljene perutanjem i pojavi područja sa alopecijom i ožiljcima. U cilju procene nejasnih oštećenja potrebno je razmotriti histopatologiju.
3.2.2.6.2. U okviru kategorije 1 korozivnih supstanci postoje tri podkategorije: podkategorija 1A kod koje se reakcija pojavljuje tokom izlaganja u trajanju od tri minuta i tokom perioda posmatranja od jedan sat, podkategorija 1B kod koje do reakcije dolazi nakon izlaganja koje traje između tri minuta i jedan sat i tokom perioda posmatranja od 14 dana i podkategorija 1C kod koje do reakcije dolazi nakon izlaganja između jednog i četiri sata i perioda posmatranja tokom narednih 14 dana.
3.2.2.6.3. Primena podataka koji se odnose na ljude opisana je u odeljcima 3.2.2.1. i 3.2.2.4, kao i u odeljacima 1.1.1.3. i 1.1.1.4. ovog priloga.
Tabela 3.2.1. Kategorija i podkategorije opasnosti za supstance korozivne za kožu
|
|
Korozivno za kožu kod > 1 od 3 životinje |
|
|
Podkategorije |
Izlaganje |
Period posmatranja |
Kategorija 1: |
1A |
≤ 3 minuta |
≤ 1 sat |
1B |
> 3 minuta ≤ 1 sat |
≤ 14 dana |
|
1C |
> 1 sat ≤ 4 sata |
≤ 14 dana |
|
3.2.2.7. Iritacija
3.2.2.7.1. Primena rezultata ispitivanja sprovedenog na životinjama radi klasifikacije u kategoriju (samo jedna kategorija) supstanci koje dovode do iritacije kože (kategorija 2) opisana je u Tabeli 3.2.2. koja je data u ovom prilogu. Primena podataka koji se odnose na ljude opisana je u odeljcima 3.2.2.1. i 3.2.2.4. kao i u odeljcima 1.1.1.3. i 1.1.1.1.4. ovog priloga. Osnovni kriterijum za kategorizaciju supstanci koje dovode do iritacije kože jeste da najmanje dve od tri ispitivane životinje imaju prosečan intenzitet iritacije kože između 2,3 i 4,0.
Tabela 3.2.2. Kriterijumi za supstance koje izazivaju iritaciju kože
Kategorija opasnosti |
Kriterijumi |
Iritativno |
(1) Prosečna vrednost između 2,3 i 4,0 za crvenilo kože/eshar ili za edem kod najmanje dve od tri ispitivane životinje nakon perioda posmatranja od 24, 48 i 72 sata po uklanjanju ispitivane supstance ili, ukoliko je reakcija odložena, tokom 3 uzastopna dana nakon pojave reakcije kože; |
3.2.2.8. Komentari na odgovore dobijene u ispitivanjima iritacije kože na životinjama
3.2.2.8.1. Rezultati ispitivanja iritativnosti na životinjama mogu biti prilično različiti, kao i kod ispitivanja supstanci koje deluju korozivno. Osnovni kriterijum za klasifikaciju neke supstance kao iritativne za kožu, kao što je prikazano u odeljku 3.2.2.7.1. ovog priloga, je srednja vrednost rezultata koji se odnose bilo na crvenilo kože/esharu ili edem kože kod najmanje dve od tri ispitivane životinje. Posebni kriterijum primenjuje se u slučajevima kada postoji jasan iritativni odgovor, ali je njegov intenzitet manji od vrednosti kriterijuma za pozitivan nalaz, npr. ispitivana supstanca se klasifikuje kao iritativna ukoliko je kod najmanje jedne od tri ispitivane životinje dobijen jasan nalaz uključujući oštećenja koja su prisutna do kraja perioda posmatranja od 14 dana. I drugi nalazi mogu zadovoljiti ovaj kriterijum. Međutim, potrebno je ustanoviti da je dobijeni nalaz rezultat izloženosti hemikaliji.
3.2.2.8.2. Reverzibilnost oštećenja kože je drugi kriterijum koji se uzima pri proceni reakcije na supstancu koja deluje iritativno. Kada je inflamacija prisutna do kraja perioda posmatranja kod dve ili više ispitivanih životinja, u vidu alopecije, hiperkeratoze, hiperplazije i perutanja, takva supstanca se klasifikuje kao iritativna za kožu.
3.2.3. Kriterijumi za klasifikaciju smeša
3.2.3.1. Klasifikacija smeša kada su dostupni podaci o svojstvima same smeše
3.2.3.1.1. Smeša se klasifikuje na osnovu kriterijuma koji se odnose na supstance, pri čemu se u obzir uzima strategija ispitivanja i procena podataka za ovu klasu opasnosti.
3.2.3.1.2. Za razliku od drugih klasa opasnosti, kod određenih smeša i supstanci postoje i alternativna ispitivanja za utvrđivanje korozivnog delovanja na kožu, koja daju tačne rezultate potrebne za klasifikaciju, a istovremeno su relativno jeftina za izvođenje. Pri razmatranju ispitivanja neke smeše, stručnjacima koji vrše klasifikaciju preporučuje se da koriste višestepeni pristup utvrđivanja kvaliteta podataka kako je dato u kriterijumima za klasifikaciju supstanci kao iritativnih ili korozivnih za kožu (odeljak 3.2.2.5. ovog priloga), da bi se istovremeno izvršila pravilna klasifikacija i izbeglo nepotrebno ispitivanje na životinjama. Smeša se smatra korozivnom za kožu (kategorija 1) ako ima pH vrednost jednaku 2 ili nižu, ili pH vrednost jednaku 11,5 ili višu. Ukoliko razmatrana acido/bazna rezerva ukazuje da supstanca ili smeša najverovatnije nemaju korozivno svojstvo uprkos niskoj ili visokoj pH vrednosti, sprovode se dodatna ispitivanja na kojima bi se ova pretpostavka potvrdila i to primenom odgovarajućeg validiranog in vitro testa.
3.2.3.2. Klasifikacija smeša kada nisu dostupni svi podaci o svojstvima same smeše: Načela premošćavanja
3.2.3.2.1. Kada sama smeša nije ispitana radi utvrđivanja njenog iritativnog/korozivnog dejstva na kožu, ali ima dovoljno podataka koji se odnose na pojedine sastojke i na slične već ispitane smeše na osnovu kojih se ova smeša može klasifikovati, ove podatke treba iskoristiti u skladu sa načelima premošćavanja koji su opisani u odeljku 1.1.3. ovog priloga.
3.2.3.3. Klasifikacija smeša kod nisu dostupni podaci za samu smešu ili za pojedine sastojke smeše
3.2.3.3.1. Da bi se iskoristili svi raspoloživi podaci u cilju klasifikacije smeše kao iritativne/korozivne za kožu, primenjuje se sledeća pretpostavka, kada je to moguće, u okviru višestepenog pristupa:
- "relevantni sastojci" smeše su oni koji su u njoj prisutni u koncentraciji od 1% (m/m za čvrste materije, tečnosti, prašinu, maglu i pare i V/V za gasove) ili više, osim ukoliko ne postoji pretpostavka (npr. u slučaju sastojaka koji imaju korozivno dejstvo na kožu) da će neki sastojak prisutan u smeši u koncentraciji manjoj od 1% biti relevantan za njenu klasifikaciju.
3.2.3.3.2. Kada se vrši klasifikacija smeše kao iritativne/korozivne za kožu na osnovu podataka koji se odnose na njene sastojke, ali ne i na smešu kao celinu, primenjuje se teorija aditivnosti, jer se smatra da svaki sastojak koji ima iritativno/korozivno dejstvo na kožu doprinosi da i smeša ima ova svojstva, prema svojoj jačini i koncentraciji u kojoj je prisutna. Faktor 10 se koristi za one korozivne sastojke koji su prisutni u koncentraciji ispod opšte granične koncentracije za klasifikaciju u kategoriju 1, ali su ipak prisutni u takvoj koncentraciji koja će doprineti da se smeša klasifikuje kao iritativna. Smeša se klasifikuje kao korozivna ili iritativna kada zbir koncentracija ovakvih komponenti prelazi koncentracioni limit.
3.2.3.3.3. Tabela 3.2.3. koja je data u ovom prilogu daje opšte granične koncentracije koje se koriste za procenu iritativnog/korozivnog delovanja smeše na kožu.
3.2.3.3.4.1. Posebna pažnja se obraća pri klasifikaciji pojedinih smeša koje sadrže supstance kao što su kiseline i baze, neorganske soli, aldehidi, fenoli i surfaktanti. Pristup koji je objašnjen u odeljcima 3.2.3.3.1. i 3.2.3.3.2. ovog priloga možda nije primenjiv u ovim slučajevima, imajući u vidu da ovakve supstance mogu imati korozivno ili iritativno dejstvo čak i kada su prisutne u koncentracijama < 1%.
3.2.3.3.4.2. Za smeše koje sadrže jake kiseline ili baze pH vrednost treba uzeti kao kriterijum (videti odeljak 3.2.3.1.2. ovog priloga) zato što je pH vrednost bolji indikator nego koncentracioni limit iz Tabele 3.2.3.
3.2.3.3.4.3. Smeša koja sadrži sastojke koji su korozivni ili iritativni za kožu i koja se ne može klasifikovati na osnovu aditivnog pristupa (Tabela 3.2.3. ovog priloga) zbog svojih hemijskih svojstava koja ovaj pristup čine neprimenjivim, klasifikuje se u kategoriju 1A, 1B ili 1C ukoliko sadrži ≥ 1% sastojka klasifikovanog u kategoriju 1A, 1B odnosno 1C ili u kategoriju 2 kada sadrži ≥ 3% sastojka sa iritativnim dejstvom. Klasifikacija smeša sa sastojcima na koje se ne mogu primeniti kriterijumi iz Tabele 3.2.3 data je u Tabeli 3.2.4. koja je data u ovom prilogu.
3.2.3.3.5. U određenim slučajevima, podaci mogu ukazivati da se korozivno/iritativno dejstvo neke supstance neće ispoljiti iako je njena koncentracija u smeši veća od opštih graničnih koncentracija datih u Tabelama 3.2.3 i 3.2.4. U tom slučaju smeša se klasifikuje na osnovu ovih podataka (videti čl. 10, 11. i 12. ovog pravilnika). U drugim slučajevima, kada se očekuje da se korozivno/iritativno dejstvo nekog sastojka neće ispoljiti kada je njegova koncentracija u smeši veća od opštih graničnih koncentracija datih u Tabelama 3.2.3 i 3.2.4, treba razmotriti mogućnost ispitivanja same smeše. Tada se za utvrđivanje kvaliteta podataka primenjuje višestepeni pristup, kao što je dato u odeljku 3.2.2.5. ovog priloga i ilustrovano na slici 3.2.1. koja je data u ovom prilogu.
3.2.3.3.6. Ukoliko postoje podaci koji ukazuju da su sastojci korozivni pri koncentraciji manjoj od 1% ili iritativni pri koncentraciji manjoj od 3%, smeša se klasifikuje u skladu sa tim.
Tabela 3.2.3. Opšte granične koncentracije za sastojke klasifikovane kao korozivne/ iritativne za kožu (kategorija 1 ili 2) koje utiču na klasifikaciju smeše kao korozivne/iritativne za kožu
Zbir sastojaka klasifikovanih kao |
Koncentracija sastojaka koja utiče na klasifikaciju smeše |
|
|
Korozivno za kožu |
Iritativno za kožu |
|
Kategorija 1 |
Kategorija 2 |
Korozivno za kožu, kategorije 1A, 1B, 1C |
≥ 5% |
≥ 1% ali < 5% |
Iritativno za kožu, kategorija 2 |
|
≥ 10% |
(10 x Korozivno za kožu, kategorije 1A, 1B, 1C) + Iritativno za kožu, kategorija 2 |
|
≥ 10% |
Napomena: Smeša se klasifikuje kao korozivna za kožu kategorije 1A, 1B, ili 1C kada zbir koncentracija svih sastojaka smeše koji su klasifikovani kao korozivni kategorije 1A, 1B ili 1C iznosi 5% ili više. Ukoliko je zbir koncentracija sastojaka kategorije 1A < 5%, ali je zbir sastojaka kategorija 1A+1B ≥ 5%, smeša se klasifikuje u kategoriju 1B. Ako je zbir koncentracija sastojaka kategorija 1A+1B < 5%, ali je zbir sastojaka iz kategorija 1A+1B+1C ≥ 5% smeša se klasifikuje u kategoriju 1C.
Tabela 3.2.4. Opšte granične koncentracije sastojaka u smeši za koje ne važi aditivni pristup i koje utiču na klasifikaciju smeše kao korozivne/iritativne za kožu
Sastojak |
Koncentracija |
Smeša klasifikovana kao korozivna/iritativna za kožu |
Kiselina, pH ≤ 2 |
≥ 1% |
Kategorija 1 |
Baza, pH ≥ 11,5 |
≥ 1% |
Kategorija 1 |
Ostali korozivni (Kategorije 1A, 1B i 1C) sastojci na koje se aditivnost ne odnosi |
≥ 1% |
Kategorija 1 |
Ostali iritativni (Kategorija 2) sastojci na koje se aditivnost ne odnosi, uključujući kiseline i baze |
≥ 3% |
Kategorija 2 |
Elementi obeležavanja
Elementi obeležavanja za supstance i smeše koje ispunjavaju uslove da budu klasifikovane u ovu klasu opasnosti dati su u Tabeli 3.2.5. koja je data u ovom prilogu.
Tabela 3.2.5. Elementi obeležavanja za korozivno oštećenje /iritaciju kože
Klasifikacija |
Kategorija 1A/1B/1C |
Kategorija 2 |
GHS piktogram opasnosti |
|
|
Reč upozorenja |
Opasnost |
Pažnja |
Obaveštenje o opasnosti |
H314: |
H315: |
Obaveštenja o merama predostrožnosti prevencija |
P260 |
P264 |
Obaveštenja o merama predostrožnosti reagovanje |
P301+P330+P331 |
P302+P352 |
Obaveštenja o merama predostrožnosti - skladištenje |
P405 |
|
Obaveštenja o merama predostrožnosti - odlaganje |
P405 |
|
3.3. Teško oštećenje oka/iritacija oka
3.3.1. Definicije
Teško oštećenje oka predstavlja oštećenje tkiva oka ili ozbiljno pogoršanje vida nakon primene ispitivane supstance na spoljašnju površinu oka, koje nije potpuno reverzibilno u periodu od 21 dana nakon primene.
Iritacija oka predstavlja nastanak promena u oku do kojih dolazi nakon primene ispitivane supstance na spoljašnju površinu oka, koje su potpuno reverzibilne u periodu od 21 dana nakon primene.
3.3.2. Kriterijumi za klasifikaciju supstanci
3.3.2.1. Sistem klasifikacije supstanci uključuje višestepeno ispitivanje i pristup proceni, kombinovanje postojećih podataka o teškim oštećenjima očnog tkiva i o iritaciji oka (uključujući i statističke podatke o dejstvu na ljude i životinje), razmatranje odnosa strukture i aktivnosti ((Q)SAR), kao i rezultata validiranih in vitro ispitivanja kako bi se izbegla nepotrebna ispitivanja na životinjama.
3.3.2.2. Pre bilo kakvog in vivo ispitivanja u vezi sa teškim oštećenjem/iritacijom oka, pregledaju se svi postojeći podaci o supstanci. Preliminarne odluke se često mogu doneti na osnovu postojećih podataka, npr. da li neki agens izaziva teško (npr. ireverzibilno) oštećenje vida. Ukoliko se supstanca može klasifikovati na osnovu ovih podataka ispitivanje nije potrebno.
3.3.2.3. Pre nego što se pristupi ispitivanju uzima se u obzir više faktora koji određuju da li neka supstanca ima potencijal da izazove teško oštećenje ili iritaciju oka. Prvo se analiziraju podaci dobijeni iz iskustava o izlaganju kod ljudi, kao i podaci dobijeni ispitivanjem na životinjama, jer ovi podaci direktno pokazuju da li neka supstanca ima efekte na oči. U pojedinim slučajevima, podaci u vezi sa strukturno sličnim jedinjenjima dovoljni su za odlučivanje o opasnosti. Tako npr. ekstremna pH vrednost ≤2 i ≥11,5 može da dovede do teškog oštećenja oka, naročito ako postoji i značajan puferski kapacitet. Za ovakve supstance se očekuje da imaju znatne efekte na oči. Pre razmatranja teškog oštećenja/iritacije oka procenjuj se korozivno dejstvo na kožu kako bi se izbeglo ispitivanje lokalnih efekata na oči za supstance koje deluju korozivno na kožu. Alternativna in vitro ispitivanja koja su validirana i prihvaćena mogu se koristiti radi klasifikacije (videti član 5. ovog pravilnika).
3.3.2.4. Prilikom određivanja potrebe za in vivo ispitivanjima iritacije oka treba koristiti sve dostupne podatke o nekoj supstanci.
Iako se ovakvi podaci mogu odnositi na procenu pojedinačnih parametara u okviru višestepenog pristupa (npr. jake baze sa ekstremnim pH vrednostima koje se smatraju supstancama sa korozivnim dejstvom), pri utvrđivanju kvaliteta podataka treba uzeti u obzir sve postojeće podatke, pogotovo ako se postojeći podaci odnose na pojedine, ali ne na sve parametre. Od primarnog značaja je stručna procena, doneta na bazi iskustva o delovanju supstance na ljude, zatim na osnovu rezultata ispitivanja iritacije kože, kao i validiranih alternativnih metoda. Kad god je moguće treba izbegavati ispitivanja supstanci sa korozivnim ili iritativnim dejstvom na životinjama.
3.3.2.5. Višestepeni pristup u proceni inicijalnih podataka, kao što je opisano u Tabeli 3.3.1. koja je data u ovom prilogu, primenjuje se kad god je moguće, ali imajući u vidu da svi elementi nisu uvek relevantni za pojedinačne slučajeve.
3.3.2.6. Ireverzibilni efekti na oko/teška oštećenja oka (kategorija 1)
3.3.2.6.1. Supstance koje imaju potencijal da ozbiljno oštete oči klasifikuju se u kategoriju 1 (ireverzibilni efekti na oko). Supstance se klasifikuju u ovu kategoriju opasnosti na osnovu ispitivanja na životinjama, u skladu sa kriterijumima datim u Tabeli 3.3.1. koja je data u ovom prilogu, što uključuje četvrti stepen oštećenja rožnjače i druge teške poremećaje (npr. destrukcija rožnjače) koji su se pojavili u bilo kom trenutku tokom ispitivanja, kao i trajno zamućenje rožnjače, diskoloraciju rožnjače, adheziju, panus, interferenciju sa funkcijom dužice ili druge efekte koji oštećuju vid. Pod trajnim oštećenjima se smatraju ona oštećenja koja nisu potpuno reverzibilna tokom uobičajenog perioda posmatranja od 21 dan. Supstance se takođe klasifikuju u kategoriju 1 ukoliko ispunjavaju kriterijume zamućenja rožnjače ≥ 3 ili iritis > 1,5 koji su uočeni na Draize testu na kunićima, uz napomenu da takva oštećenja obično nisu reverzibilna tokom perioda posmatranja od 21 dan.
Tabela 3.3.1. Kriterijumi za ireverzibilne efekte na oko
Kategorija opasnosti |
Kriterijumi |
Ireverzibilni efekti na oko (Kategorija 1) |
Ukoliko supstanca, kada se primeni u oko jedne životinje, dovodi do: |
3.3.2.6.2. Korišćenje podataka dobijenih na osnovu delovanja na ljude razmotreno je u odeljcima 3.3.2.1. i 3.3.2.4, kao i u odeljcima 1.1.1.3, 1.1.1.4. i 1.1.1.5. ovog priloga.
3.3.2.7. Reverzibilni efekti na oko (Kategorija 2)
3.3.2.7.1. Supstance koje mogu dovesti do reverzibilne iritacije oka klasifikuju se u kategoriju 2 na osnovu rezultata ispitivanja na životinjama i u skladu sa kriterijumima navedenim u Tabeli 3.3.2. koja je data u ovom prilogu.
Tabela 3.3.2. Kriterijumi za reverzibilne efekte na oko
Kategorija opasnosti |
Kriterijumi |
Iritativno za oko |
Ukoliko supstanca, kada se primeni u oko životinje, dovodi do: |
3.3.2.7.2. Za one supstance kod kojih je izražena varijabilnost u reakciji ispitivanih životinja ovi podaci se uzimaju u obzir pri klasifikaciji.
3.3.3. Kriterijumi za klasifikaciju smeša
3.3.3.1. Klasifikacija smeša kada su dostupni podaci o svojstvima same smeše
3.3.3.1.1. Smeša se klasifikuje u skladu sa kriterijumima koji važe za supstance i na osnovu strategija za ispitivanje i procenu koje se koriste za ove klase opasnosti.
3.3.3.1.2. Za razliku od drugih klasa opasnosti, za utvrđivanje da li neka supstanca ima korozivno dejstvo na kožu postoje i alternativna ispitivanja koja se primenjuju kod određenih tipova supstanci i smeša i koja daju tačne podatke potrebne za klasifikaciju. Ova alternativna ispitivanja su jeftina i relativno jednostavna za izvođenje. Kada se razmatra ispitivanje neke smeše, preporučuje se da se primeni višestepeni pristup pri utvrđivanju kvaliteta podataka za klasifikaciju neke supstance u odnosu na svojstvo da izazove korozivno oštećenje kože, teško oštećenje oka i/ili iritaciju oka, kako bi se izvršila pravilna klasifikacija i istovremeno izbeglo nepotrebno ispitivanje na životinjama. Smatra se da smeša dovodi do korozivnog oštećenja oka (kategorija 1) kada ima pH vrednost ≤ 2,0 ili ≥ 11,5. Ukoliko razmatranje acido/bazne rezerve ukazuje da supstanca ili smeša najverovatnije nema potencijal da izazove teško oštećenje oka uprkos niskoj ili visokoj pH vrednosti, treba sprovesti dodatna ispitivanja koja bi potvrdila ovu pretpostavku i to prvenstveno primenom odgovarajućih validiranih in vitro testova.
3.3.3.2. Klasifikacija smeša kada nisu dostupni podaci o svojstvima same smeše: Načela premošćavanja
3.3.3.2.1. Kada sama smeša nije ispitana radi utvrđivanja njenog korozivnog dejstva na kožu ili potencijala da dovede do teškog oštećenja oka ili iritacije, ali ima dovoljno podataka koji se odnose na pojedinačne sastojke i na slične već ispitane smeše na osnovu kojih se ova smeša može odgovarajuće klasifikovati, ovi podaci koriste se u skladu sa načelima premošćavanja iz odeljka 1.1.3. ovog priloga.
3.3.3.3. Klasifikacija smeša kada su dostupni podaci za sve ili samo za neke sastojke smeše
3.3.3.3.1. Da bi se iskoristili svi raspoloživi podaci u postupku klasifikacije smeše u klasu opasnosti teško oštećenje oka/iritacija oka, primenjuje se sledeća pretpostavka, kada je to moguće, u okviru višestepenog pristupa:
"Relevantni sastojci" smeše su oni koji su u njoj sadržani u koncentraciji od 1% (m/m za čvrste smeše, tečnosti, prašinu, maglu i pare i V/V za gasove) ili većoj, osim ukoliko ne postoji razlog (npr. u slučaju sastojaka koji imaju korozivno dejstvo) da se neki sastojak prisutan u smeši u koncentraciji manjoj od 1% uzme kao relevantan za njenu klasifikaciju.
3.3.3.3.2. Pri klasifikaciji smeša u odnosu na teško oštećenje oka/iritaciju oka, kada su dostupni podaci koji se odnose na sastojke, ali ne i na smešu kao celinu, procena se zasniva na teoriji aditivnosti, tako da svaki korozivni ili iritativni sastojak doprinosi ukupnim iritativnim ili korozivnim svojstvima smeše srazmerno svojoj jačini i koncentraciji. Faktor 10 se koristi za korozivne supstance kada su one prisutne u koncentraciji ispod opšte granične koncentracije za klasifikaciju u kategoriju 1, ali su prisutne u takvoj koncentraciji koja će doprineti da se smeša klasifikuje kao iritativna. Smeša se klasifikuje kao smeša koja izaziva teško oštećenje oka ili iritaciju oka kada zbir koncentracija ovakvih sastojaka prelazi granične koncentracije.
3.3.3.3.3. U Tabeli 3.3.3. koja je data u ovom prilogu date su opšte granične koncentracije na osnovu kojih se smeša klasifikuje kao smeša koja izaziva teško oštećenje oka ili iritaciju oka.
3.3.3.3.4.1. Posebna pažnja se obraća pri klasifikaciji pojedinih smeša koje sadrže supstance kao što su kiseline i baze, neorganske soli, aldehidi, fenoli i surfaktanti. Pristup koji je objašnjen u odeljcima 3.3.3.3.1. i 3.3.3.3.2. ovog priloga možda nije primenjiv u ovim slučajevima imajući u vidu da ovakve supstance mogu imati korozivno ili iritativno dejstvo čak i kada su prisutne u koncentracijama < 1%.
3.3.3.3.4.2. Za smeše koje sadrže jake kiseline ili baze, kriterijum za klasifikaciju treba da bude pH vrednost (videti odeljak 3.3.2.3. ovog priloga) pošto je pH vrednost bolji pokazatelj za teško oštećenje oka nego opšta granična koncentracija data u Tabeli 3.3.3. koja je data u ovom prilogu.
3.3.3.3.4.3. Smeša koja sadrži sastojke sa korozivnim/iritativnim dejstvom, a koja se ne može klasifikovati na osnovu aditivnosti (Tabela 3.3.3.) zbog hemijskih svojstava koja čine ovaj pristup neprimenjivim, treba da bude klasifikovana u kategoriju 1 za efekte na oko ukoliko sadrži ≥1% sastojka sa korozivnim dejstvom i u kategoriju 2 kada sadrži ≥3% sastojka sa iritativnim dejstvom. Klasifikacija smeša sa sastojcima na koje se ne mogu primeniti kriterijumi iz Tabele 3.3.3. objedinjeni su u Tabeli 3.3.4. koja je data u ovom prilogu.
3.3.3.3.5. U pojedinim slučajevima, podaci o određenom sastojku mogu pokazati da se njegovi reverzibilni/ireverzibilni efekti na oko neće ispoljiti kada je koncentracija tog sastojka u smeši veća od opšte granične koncentracije date u Tabelama 3.3.3 i 3.3.4. ovog priloga. U tim slučajevima smeša se klasifikuje na osnovu ovih podataka. U drugim slučajevima kada se očekuje da neki sastojak neće izazvati korozivno oštećenje kože/iritaciju kože ili reverzibilne/ireverzibilne efekte na oko, ukoliko je koncentracija tog sastojka u smeši veća od opšte granične koncentracije date u Tabelama 3.3.3 i 3.3.4, razmatra se mogućnost ispitivanja same smeše. U tim slučajevima, pri utvrđivanju kvaliteta podataka primenjuje se višestepeni pristup.
3.3.3.3.6. Ukoliko postoje podaci koji ukazuju da sastojci mogu biti korozivni ili iritativni u koncentraciji od < 1% (korozivno) ili < 3% (iritativno) smeša se klasifikuje na osnovu tih podataka.
Tabela 3.3.3. Opšte granične koncentracije sastojaka smeše koji su klasifikovani u kategoriju 1 za korozivno oštećenje kože,
odnosno u kategoriju 1 ili 2 za efekte na oko koji impliciraju klasifikaciju smeše u odnosu na efekte na oko
(kategorija 1 ili 2)
Zbir sastojaka klasifikovanih kao |
Koncentracija koja utiče na klasifikaciju smeše kao |
|
Ireverzibilni efekti na oko |
Reverzibilni efekti na oko |
|
Kategorija 1 |
Kategorija 2 |
|
Efekti na oko, kategorija 1 |
≥ 3% |
≥ 1% ali < 3% |
Efekti na oko, kategorija 2 |
|
≥ 10% |
(10 x Efekti na oko, kategorija 1) + Efekti na oko, kategorija 2 |
|
≥ 10% |
Korozivno oštećenje kože, kategorije 1A, 1B, 1C + Efekti na oko, kategorija 1 |
≥ 3% |
≥ 1% ali < 3% |
10 x (Korozivno oštećenje kože, kategorija 1A, 1B, 1C + Efekti na oko, kategorija 1) + Efekti na oko, kategorija 2 |
|
≥ 10% |
Tabela 3.3.4. Opšte granične koncentracije sastojaka u smeši za koje ne važi aditivni pristup i koje utiču na klasifikaciju smeše kao opasne za oko
Sastojak |
Koncentracija |
Smeša klasifikovana kao opasna za oko |
Kiselina, pH ≤ 2 |
≥ 1% |
Kategorija 1 |
Baza, pH ≥ 11,5 |
≥ 1% |
Kategorija 1 |
Ostali korozivni sastojci (Kategorija 1) na koje se aditivnost ne može primeniti |
≥ 1% |
Kategorija 1 |
Ostali iritativni sastojci (Kategorija 2) na koje se aditivnost ne može primeniti, uključujući kiseline i baze |
≥ 3% |
Kategorija 2 |
3.3.4. Elementi obeležavanja
Elementi obeležavanja za supstance i smeše koje ispunjavaju uslove da budu klasifikovane u ovu klasu opasnosti dati su u Tabeli 3.3.5. koja je data u ovom prilogu.
Tabela 3.3.5. Elementi obeležavanja za teško oštećenje oka / iritaciju oka
Klasifikacija |
Kategorija 1 |
Kategorija 2 |
GHS piktogram opasnosti |
|
|
Reč upozorenja |
Opasnost |
Pažnja |
Obaveštenje o opasnosti |
H318: |
H319: |
Obaveštenja o merama predostrožnosti prevencija |
P280 |
P264 |
Obaveštenja o merama predostrožnosti reagovanje |
P305+P351+P338 |
P305+P351+P338 |
Obaveštenja o merama predostrožnosti skladištenje |
|
|
Obaveštenja o merama predostrožnosti odlaganje |
|
|
3.4. Senzibilizacija respiratornih organa/senzibilizacija kože
3.4.1. Definicije i opšta razmatranja
3.4.1.1. Senzibilizator respiratornih organa je supstanca ili smeša koja nakon udisanja dovodi do preosetljivosti respiratornih puteva.
3.4.1.2. Senzibilizator kože je supstanca ili smeša koja dovodi do alergijskog odgovora nakon kontakta sa kožom.
3.4.1.3. Senzibilizacija respiratornih organa ili kože odvija se u dve faze: prva faze je faza indukcije imunološke memorije izlaganjem pojedinca alergenu. Druga faza je provokacija, tj. produkcija ćelijskog ili antitelima posredovanog alergijskog odgovora nakon izlaganja alergenu.
3.4.1.4. Opšti model indukcije koja je praćena provokacijom je zajednički za senzibilizaciju kože i senzibilizaciju respiratornih organa. Za senzibilizaciju kože neophodna je faza indukcije jer tokom te faze imuni sistem uči da reaguje; klinički simptomi se tada mogu pojaviti ako je izlaganje alergenu trajalo dovoljno dugo da bi izazvalo vidljivu reakciju na koži (faza provokacije). Prediktivni testovi obično slede ovu šemu, u kojoj je faza indukcije, odgovor koji se meri standardizovanom fazom provokacije, koji tipično uključuje patch test. Test procene lokalnih limfnih čvorova je izuzetak i direktno meri indukcioni odgovor. Dokazi o senzibilizaciji kože kod ljudi se obično procenjuju na osnovu dijagnostičkih patch testova.
3.4.1.5. Kod senzibilizacije kože, kao i kod senzibilizacije respiratornih organa, za provokaciju su potrebni niži nivoi nego za indukciju. Odredbe o načinu upozoravanja osetljivih osoba na prisustvo nekog alergena u smeši mogu se naći u Prilogu 6. Deo 2. odeljak 2.8. ovog pravilnika.
3.4.1.6. Klasa opasnosti Senzibilizacija respiratornih organa/senzibilizacija kože deli se na:
- Senzibilizaciju respiratornih organa;
- Senzibilizaciju kože.
3.4.2. Kriterijumi za klasifikaciju supstanci
3.4.2.1. Senzibilizatori respiratornih organa
3.4.2.1.1. Kategorije opasnosti
3.4.2.1.1.1. Kada nema dovoljno podataka za klasifikaciju u podkategorije, senzibilizatori respiratornih organa klasifikuju se u Kategoriju 1.
3.4.2.1.1.2. Kada je dostupno dovoljno podataka, precizna procena u skladu sa odeljkom 3.4.2.1.1.3. ovog priloga omogućava klasifikaciju senzibilizatora respiratornih organa u podkategoriju 1A, jaki senzibilizatori, ili u podkategoriju 1B, ostali senzibilizatori respiratornih organa.
3.4.2.1.1.3. Efekti uočeni kod ljudi ili životinja obično potvrđuju klasifikaciju pristupom utvrđivanja kvaliteta podataka za senzibilizatore respiratornih organa. Supstance mogu da se klasifikuju u jednu od dve kategorije, 1A ili 1B, korišćenjem pristupa utvrđivanja kvaliteta podataka u skladu sa kriterijumima datim u Tabeli 3.4.1. koja je data u ovom prilogu i na osnovu pouzdanih i kvalitetnih dokaza kod ljudi iz prikaza slučajeva ili epidemioloških studija odnosno zapažanja iz odgovarajućih studija na eksperimentalnim životinjama.
3.4.2.1.1.4. Supstance se klasifikuju kao senzibilizatori respiratornih organa u skladu sa kriterijumima datim u Tabeli 3.4.1. koja je data u ovom prilogu.
Tabela 3.4.1. Kategorija i podkategorije opasnosti za senzibilizatore respiratornih organa
Kategorija opasnosti |
Kriterijumi |
Kategorija 1 |
Kada nema dovoljno podataka za klasifikaciju u podkategorije supstanca se klasifikuje kao senzibilizator respiratornih organa (Kategorija 1) na osnovu sledećih kriterijuma: |
Podkategorija 1A: |
Supstance pokazuju visoku učestalost pojave senzibilizacije kod ljudi ili je verovatna pojava visoke stope senzibilizacije kod ljudi na osnovu ispitivanja na životinjama ili drugih ispitivanja (*). Može se uzeti u obzir i ozbiljnost reakcije. |
Podkategorija 1B: |
Supstance pokazuju malu do umerenu učestalost pojave senzibilizacije kod ljudi ili verovatna pojava niske ili umerene stope senzibilizacije kod ljudi na osnovu ispitivanja na životinjama ili drugih ispitivanja (*). Može se uzeti u obzir i ozbiljnost reakcije. |
Napomena (*): U ovom trenutku nisu dostupni prihvaćeni i potvrđeni modeli ispitivanja respiratorne preosetljivosti kod životinja. U određenim slučajevima podaci dobijeni iz studija na životinjama mogu da obezbede korisne informacije u proceni kvaliteta podataka. |
|
3.4.2.1.2. Podaci dobijeni na osnovu iskustava kod ljudi
3.4.2.1.2.1. Dokaz da neka supstanca može dovesti do specifične respiratorne preosetljivosti obično je zasnovan na iskustvima kod ljudi. U skladu sa ovim, preosetljivost se obično ispoljava kao astma, ali to mogu biti i druge reakcije preosetljivosti kao što su rinitis, odnosno konjuktivitis i alveolitis, koje takođe treba uzeti u obzir. Klinička slika, u tim slučajevima, ukazuje na alergijsku reakciju, međutim imunološki mehanizmi se ne moraju ispoljiti.
3.4.2.1.2.2. Kada se razmatraju podaci dobijeni na osnovu iskustva kod ljudi, za klasifikaciju supstance neophodno je razmotriti i:
1) veličinu izložene populacije;
2) stepen izloženosti.
Primena podataka dobijenih na osnovu iskustva kod ljudi opisana je u odeljcima 1.1.1.3, 1.1.1.4. i 1.1.1.5. ovog priloga.
3.4.2.1.2.3. Pomenuti dokazi mogu biti:
1) klinička anamneza i podaci odgovarajućeg testa funkcije pluća u vezi sa izlaganjem supstanci, potvrđenim i drugim dodatnim dokazima koji mogu da uključuju:
- in vivo imunološki test (npr. ubodni kožni ("prick") test);
- in vitro imunološki test (npr. serološke analize);
- studije koje upućuju na druge reakcije preosetljivosti gde imunološki mehanizmi delovanja nisu dokazani, npr. ponovljena blaga iritacija, farmakološki posredovani efekti;
- podaci o supstancama slične hemijske strukture koje dovode do respiratorne preosetljivosti;
2) podaci sa jednog ili više bronhijalnih testova provokacije supstancama, na osnovu prihvaćenih procedura za utvrđivanje specifičnih reakcija preosetljivosti.
3.4.2.1.2.4. Klinička anamneza sadrži, pored medicinskih podataka, i podatke o profesionalnoj anamnezi kako bi se uspostavila veza između izlaganja određenoj supstanci i nastanka respiratorne preosetljivosti. Relevantni podaci sadrže informacije o postojanju rizika i kod kuće i na radnom mestu, nastanak i razvoj bolesti, porodičnu istoriju bolesti i medicinsku anamnezu pacijenta čiji se slučaj razmatra. Medicinska anamneza sadrži i podatke o drugim alergijskim reakcijama ili oboljenjima respiratornog trakta od detinjstva, kao i anamnezu o konzumaciji duvana.
3.4.2.1.2.5. Pozitivni rezultati testa bronhijalne provokacije smatraju se dovoljnim za klasifikaciju supstance. Mnoga od navedenih ispitivanja sprovedena su u praksi.
3.4.2.1.3. Ispitivanja na životinjama
3.4.2.1.3.1. Podaci dobijeni u odgovarajućim ispitivanjima na životinjama(14) koji mogu da ukažu na potencijal supstance da kod ljudi izazove senzibilizaciju nakon udisanja(15) mogu da sadrže:
1) vrednosti imunoglobulina E (IgE) i drugih specifičnih imunoloških parametara kod miševa;
2) specifične plućne odgovore kod zamoraca.
_________
(14) U ovom trenutku nisu dostupni prihvaćeni i potvrđeni modeli ispitivanja respiratorne preosetljivosti kod životinja. U određenim slučajevima podaci dobijeni iz studija na životinjama mogu da obezbede korisne informacije za procenu kvaliteta podataka.
(15) Mehanizmi kojim supstance izazivaju simptome astme još uvek nisu u potpunosti poznati. Iz preventivnih razloga, ovakve supstance klasifikuju se kao senzibilizatori respiratornih organa. Ipak, ako se na osnovu dostupnih podataka ustanovi da ove supstance izazivaju simptome astme samo kod ljudi sa bronhijalnom preosetljivošću, ne treba ih klasifikovati kao senzibilizatore respiratornih organa.
3.4.2.2. Senzibilizatori kože
3.4.2.2.1. Kategorije opasnosti
3.4.2.2.1.1. Kada nema dovoljno podataka za klasifikaciju u podkategorije, senzibilizatori kože klasifikuju se u Kategoriju 1.
3.4.2.2.1.2. Kada je dostupno dovoljno podataka, precizna procena u skladu sa odeljkom 3.4.2.2.1.3. ovog priloga omogućava klasifikaciju senzibilizatora kože u podkategoriju 1A, jaki senzibilizatori, ili u podkategoriju 1B, ostali senzibilizatore kože.
3.4.2.2.1.3. Efekti uočeni kod ljudi ili životinja obično potvrđuju klasifikaciju pristupom utvrđivanja kvaliteta podataka za senzibilizatore kože kao što je opisano u odeljku 3.4.2.2.2. ovog priloga. Supstance mogu da se klasifikuju u jednu od dve kategorije, 1A ili 1B, korišćenjem pristupa utvrđivanja kvaliteta podataka u skladu sa kriterijumima koji su dati u Tabeli 3.4.2. koja je data u ovom prilogu i na osnovu pouzdanih i kvalitetnih dokaza kod ljudi iz prikaza slučajeva ili epidemioloških studija odnosno zapažanja iz odgovarajućih studija na eksperimentalnim životinjama u skladu sa vrednostima koje su date u odeljcima 3.4.2.2.2.1. i 3.4.2.2.3.2. ovog priloga, za podkategoriju 1A i odeljcima 3.4.2.2.2.2. i 3.4.2.2.3.3. ovog priloga za podkategoriju 1B.
3.4.2.2.1.4. Supstance se klasifikuju kao senzibilizatori kože u skladu sa kriterijumima datim u Tabeli 3.4.2. koja je data u ovom prilogu.
Tabela 3.4.2. Kategorija i podkategorije opasnosti za senzibilizatore kože
Kategorija opasnosti |
Kriterijumi |
Kategorija 1 |
Kada nema dovoljno podataka za klasifikaciju u podkategorije supstanca se klasifikuje kao senzibilizator kože (Kategorija 1) na osnovu sledećih kriterijuma: |
Podkategorija 1A: |
Za supstance koje pokazuju visoku učestalost pojave senzibilizacije kod ljudi odnosno jak efekat kod životinja može se pretpostaviti da imaju potencijal da izazovu značajnu senzibilizaciju kod ljudi. Može se uzeti u obzir i ozbiljnost reakcije. |
Podkategorija 1B: |
Za supstance koje pokazuju malu do umerenu učestalost pojave senzibilizacije kod ljudi odnosno slab do umeren efekat kod životinja može se pretpostaviti da imaju potencijal da izazovu senzibilizaciju kod ljudi. Može se uzeti u obzir i ozbiljnost reakcije. |
3.4.2.2.2. Podaci dobijeni na osnovu nalaza kod ljudi
3.4.2.2.2.1. Podaci dobijeni na osnovu nalaza kod ljudi za klasifikaciju u podkategoriju 1A mogu da budu:
1) pozitivna reakcija pri ≤ 500 µg/cm2 (primenom testa human repeat-insult patch test (u daljem tekstu: HRIPT) i testa historical maximization tests (u daljem tekstu: HMT) - prag indukcije);
2) Podaci iz dijagnostičkog "patch" testa kada postoji relativno velika i značajna učestalost reakcija kod određenog dela populacije u odnosu na relativno malu izloženost;
3) podaci iz drugih epidemioloških studija kada postoji relativno velika i značajna učestalost alergijskog kontaktnog dermatitisa u odnosu na relativno malu izloženost.
3.4.2.2.2.2. Podaci dobijeni na osnovu nalaza kod ljudi za klasifikaciju u podkategoriju 1B mogu da budu:
1) pozitivna reakcija pri > 500 µg/cm2 (HRIPT, HMT - prag indukcije);
2) podaci iz dijagnostičkog "patch" testa kada postoji relativno mala ali značajna učestalost reakcija kod određenog dela populacije u odnosu na relativno veliku izloženost;
3) podaci iz drugih epidemioloških studija kada postoji relativno mala ali značajna učestalost alergijskog kontaktnog dermatitisa u odnosu na relativno veliku izloženost.
Primena podataka dobijenih na osnovu nalaza kod ljudi data je u odeljcima 1.1.1.3, 1.1.1.4. i 1.1.1.5. ovog pravilnika.
3.4.2.2.3. Ispitivanja na životinjama
3.4.2.2.3.1. Za Kategoriju 1, kada se koristi metoda ispitivanja senzibilizacije kože sa adjuvansom, pozitivnim odgovorom smatra se reakcija kod najmanje 30% ispitivanih životinja. Za metodu ispitivanja na zamorcima bez adjuvansa pozitivnim odgovorom smatra se reakcija kod najmanje 15% ispitivanih životinja. Za Kategoriju 1, indeks stimulacije 3 i više smatra se pozitivnim odgovorom u Testu lokalnih limfnih čvorova. Metode ispitivanja za senzibilizaciju kože opisane su u propisu kojim se uređuju metode ispitivanja opasnih svojstava hemikalija, i to: metoda ispitivanja B.6. Senzibilizacija kože (Test maksimizacije na zamorcima i Buehler test) i metoda ispitivanja B.42. (Senzibilizacija kože: test lokalnih limfnih čvorova). Druge metode mogu se koristiti ako su potvrđene i za njihovu upotrebu postoji naučna opravdanost. Na primer, Test oticanja uha miša (Mouse Ear Swelling Test, MEST) može da bude pouzdano skrining ispitivanje za otkrivanje srednje do jakih senzibilizatora i može da se koristi kao prva faza u proceni potencijala za senzibilizaciju kože.
3.4.2.2.3.2. Podaci dobijeni iz ispitivanja na životinjama za klasifikaciju u podkategoriju 1A mogu da budu podaci sa vrednostima navedenim u Tabeli 3.4.3. ovog priloga.
Tabela 3.4.3. Podaci dobijeni iz ispitivanja na životinjama za klasifikaciju u podkategoriju 1A
Ispitivanje |
Kriterijum |
Test lokalnih limfnih čvorova |
EC3 vrednost ≤ 2% |
Test maksimizacije na zamorcima |
≥ 30% reaguje na ≤ 0,1% intradermalne indukcione doze ili |
Buehler test |
≥ 15% reaguje na ≤ 0,2% topikalne indukcione doze ili |
3.4.2.2.3.3. Podaci dobijeni iz ispitivanja na životinjama za klasifikaciju u podkategoriju 1B mogu da budu podaci sa vrednostima navedenim u Tabeli 3.4.4. ovog priloga.
Tabela 3.4.4. Podaci dobijeni iz ispitivanja na životinjama za klasifikaciju u podkategoriju 1B
Ispitivanje |
Kriterijum |
Test lokalnih limfnih čvorova |
EC3 vrednost > 2% |
Test maksimizacije na zamorcima |
≥ 30% do < 60% reaguje na > 0,1% do ≤ 0,1% intradermalne indukcione doze ili |
Buehler test |
≥ 15% do < 60% reaguje na > 0,2% do ≤ 20% topikalne indukcione doze ili |
3.4.2.2.4. Posebna uputstva
3.4.2.2.4.1. Za klasifikaciju supstance potreban je najmanje jedan od sledećih podataka u pristupu utvrđivanja kvaliteta podataka:
1) pozitivni rezultati "patch" testa, dobijeni na više od jednoj dermatološkoj klinici;
2) epidemiološke studije koje ukazuju na kontaktni dermatitis izazvan tom supstancom; situacije u kojima visok procenat osoba izloženih datoj supstanci ispoljava karakteristične simptome posmatraju se sa posebnom pažnjom, čak i kada je broj takvih slučajeva mali;
3) pozitivni rezultati dobijeni odgovarajućim studijama na životinjama;
4) pozitivni rezultati dobijeni u eksperimentalnim studijama kod ljudi;
5) dokumentovani slučajevi alergijskog kontaktnog dermatitisa dobijeni na više od jednoj dermatološkoj klinici;
6) može se uzeti u obzir i ozbiljnost reakcije.
3.4.2.2.4.2. Podaci dobijeni u ispitivanjima na životinjama obično su pouzdaniji od podataka o izlaganju ljudi. Međutim, kada su dostupni podaci iz oba izvora i kada postoji neslaganje u rezultatima, procenjuju se kvalitet i pouzdanost i jednih i drugih podataka u svakom pojedinačnom slučaju kako bi se donela odluka o klasifikaciji. U najvećem broju slučajeva podaci o delovanju supstance na ljude u cilju klasifikacije opasnosti nisu dobijeni u kontrolisanim eksperimentima sa dobrovoljcima, već kao deo procene rizika u cilju potvrde odsustva efekata uočenih u eksperimentima na životinjama. Pozitivni dokazi o senzibilizaciji kože kod ljudi obično se izvode iz pojedinačnih slučajeva ili drugih, manje pouzdanih studija. Podaci koji se odnose na ljude pažljivo se procenjuju, jer učestalost slučajeva, pored opasnih svojstava supstance, zavisi i od faktora kao što su okolnosti u kojima je došlo do izlaganja, bioraspoloživost, individualna predispozicija i preduzete preventivne mere. Negativni nalazi kod ljudi ne mogu se automatski koristiti da negiraju pozitivne rezultate ispitivanja na životinjama. Kod oba izvora podataka, potrebno je razmotriti uticaj nosača koji se koristi.
3.4.2.2.4.3. Ukoliko nijedan od navedenih uslova nije ispunjen, supstanca se ne klasifikuje kao senzibilizator kože. Kombinacija dva ili više indikatora senzibilizacije kože može promeniti odluku o klasifikaciji i tada se o klasifikaciji odlučuje razmatranjem svakog slučaja pojedinačno.
Indikatori senzibilizacije kože su:
1) izolovane epizode alergijskog kontaktnog dermatitisa;
2) epidemiološke studije ograničenog statističkog značaja npr. kada pojedinačni slučajevi, bias ili slučajevi koji odstupaju nisu odbačeni sa odgovarajućom pouzdanošću;
3) podaci dobijeni u ispitivanjima na životinjama, sprovedenim u skladu sa propisima, koji ne zadovoljavaju kriterijume za klasifikaciju kao što je opisano u odeljku 3.4.2.2.3. ovog priloga, ali koji su dovoljno blizu granice da se mogu smatrati značajnim za klasifikaciju;
4) pozitivni rezultati dobijeni primenom nestandardnih metoda;
5) pozitivni rezultati na ispitivanjima sa strukturnim analozima.
3.4.2.2.4.4. Imunološka kontaktna urtikarija (koprivnjača)
Supstance koje zadovoljavaju kriterijume da budu klasifikovane kao senzibilizatori respiratornih organa mogu uzrokovati i imunološku kontaktnu urtikariju (koprivnjaču). Zbog toga je potrebno razmotriti i njihovu klasifikaciju kao senzibilizatora kože. Za supstance koje dovode do pojave imunološke kontaktne urtikarije, ali koje ne ispunjavaju kriterijume za klasifikaciju kao senzibilizatori respiratornih organa, razmatra se mogućnost klasifikacije kao senzibilizatora kože.
Za sada nema odgovarajućeg modela na životinjama za identifikaciju supstanci koje dovode do pojave imunološke kontaktne urtikarije. Zbog toga se klasifikacija obično zasniva na nalazima kod ljudi, koji će biti slični podacima dobijenim za senzibilizaciju kože.
3.4.3. Kriterijumi za klasifikaciju smeša
3.4.3.1. Klasifikacija smeša kada su dostupni podaci o svojstvima same smeše
3.4.3.1.1. Kada za smeše postoje pouzdani i kvalitetni podaci koji se odnose na ljude ili odgovarajuće studije na eksperimentalnim životinjama, kao što je opisano u kriterijumima za supstance, onda se smeša može klasifikovati na osnovu utvrđivanja kvaliteta ovih podataka. Pri utvrđivanju kvaliteta podataka kod smeša treba obratiti pažnju na to da primenjene doze mogu biti takve da se na osnovu dobijenih rezultata ne može izvesti nedvosmislen zaključak.
3.4.3.2. Klasifikacija smeša kada nisu dostupni podaci o svojstvima same smeše: Načela premošćavanja
3.4.3.2.1. Kada sama smeša nije ispitana radi utvrđivanja njenih svojstava senzibilizacije, ali postoji dovoljno podataka o pojedinačnim sastojcima i podataka o sličnim smešama, takvih da se na odgovarajući način okarakterišu opasnosti, ove podatke treba koristiti na osnovu načela premošćavanja datih u odeljku 1.1.3. ovog priloga.
3.4.3.3. Klasifikacija smeša kada su dostupni podaci za sve ili samo za neke njene sastojke
3.4.3.3.1. Smeša se klasifikuje kao senzibilizator respiratornih organa ili kože kada je barem jedan njen sastojak tako klasifikovan i prisutan u koncentraciji istoj ili većoj od opšte granične koncentracije, kao što je dato u Tabeli 3.4.5. koja je data u ovom odeljku.
3.4.3.3.2. Neke supstance koje su klasifikovane kao senzibilizatori respiratornih organa ili kože kod osoba koje su već senzibilisane na supstancu ili smešu mogu izazvati reakciju, ukoliko su prisutne u smešama u koncentracijama koje su ispod koncentracija datih u Tabeli 3.4.5. koja je data u ovom odeljku.
Tabela 3.4.5. Opšte granične koncentracije za sastojke smeše klasifikovane kao senzibilizatori kože ili respiratornih organa, koje utiču na klasifikaciju smeše
Sastojak klasifikovan kao |
Opšte granične koncentracije koje utiču na klasifikaciju smeše kao |
||
Senzibilizator respiratornih organa |
Senzibilizator kože |
||
čvrsto/tečnost |
gas |
sva fizička stanja |
|
Senzibilizator respiratornih organa |
≥ 1,0% |
≥ 0,2% |
- |
Senzibilizator respiratornih organa |
≥ 0,1% |
≥ 0,1% |
- |
Senzibilizator respiratornih organa |
≥ 1,0% |
≥ 0,2% |
- |
Senzibilizator kože |
- |
- |
≥ 1,0% |
Senzibilizator kože |
- |
- |
≥ 0,1% |
Senzibilizator kože |
- |
- |
≥ 1,0% |
Tabela 3.4.6. Granične koncentracije za izdvajanje sastojaka smeše
Sastojak klasifikovan kao |
Granične koncentracije za izdvajanje |
||
Senzibilizator respiratornih organa |
Senzibilizator kože |
||
čvrsto/tečnost |
gas |
sva fizička stanja |
|
Senzibilizator respiratornih organa |
≥ 0,1% (Napomena 1) |
≥ 0,1% |
- |
Senzibilizator respiratornih organa |
≥ 0,01% |
≥ 0,01% (Napomena 1) |
- |
Senzibilizator respiratornih organa |
≥ 0,1% (Napomena 1) |
≥ 0,1% |
- |
Senzibilizator kože |
- |
- |
≥ 0,1% |
Senzibilizator kože |
- |
- |
≥ 0,01% |
Senzibilizator kože |
- |
- |
≥ 0,1% |
Napomena 1: Ova granična koncentracija za izdvajanje koristi se u slučaju kada je potrebno posebno obeležavanje prema zahtevima datim u Prilogu 6. odeljak 2.10. ovog pravilnika, da bi se zaštitile osobe koje su već senzibilisane. Za smešu koja sadrži sastojak iznad ove koncentracije neophodan je bezbednosni list. Za supstance koje izazivaju senzibilizaciju, a za koje su propisane specifične granične koncentracije manje od 0,1%, granična koncentracija za izdvajanje određuje se kao deseti deo specifične granične koncentracije.
3.4.4. Elementi obeležavanja
3.4.4.1. Elementi obeležavanja za supstance i smeše koje ispunjavaju uslove da budu klasifikovane u ovu klasu opasnosti dati su u Tabeli 3.4.7. koja je data u ovom prilogu.
Tabela 3.4.7. Elementi obeležavanja za senzibilizaciju respiratornih organa ili kože
Klasifikacija |
Senzibilizacija respiratornih organa |
Senzibilizacija kože |
Senzibilizacija respiratornih organa, |
Senzibilizacija respiratornih organa, |
|
GHS piktogram opasnosti |
|
|
Reč upozorenja |
Opasnost |
Pažnja |
Obaveštenje o opasnosti |
H334: |
H317: |
Obaveštenja o merama predostrožnosti - prevencija |
P261 |
P261 |
Obaveštenja o merama predostrožnosti - reagovanje |
P304+P341 |
P302+P352 |
Obaveštenja o merama predostrožnosti - skladištenje |
|
|
Obaveštenja o merama predostrožnosti - odlaganje |
P501 |
P501 |
3.5. Mutagenost germinativnih ćelija
3.5.1. Definicije i opšta razmatranja
3.5.1.1. Mutacija predstavlja trajnu promenu u broju i strukturi genetskog materijala u ćeliji. Termin "mutacija" se odnosi i na nasledne genetske promene koje se mogu manifestovati na nivou fenotipa, kao i na promene strukture DNK (uključujući i specifične promene baznih parova i hromozomske translokacije). Termini "mutageno" i "mutagen" će se koristiti za supstance i smeše koje dovode do povećanja broja mutacija kod populacije ćelija, odnosno organizama.
3.5.1.2. Opšti termini "genotoksičnost" i "genotoksično" odnose se na supstance i smeše ili procese koji menjaju strukturu, sadržaj informacija ili segregaciju DNK, uključujući i one supstance i smeše koje oštećuju DNK interferencijom sa normalnim procesima replikacije ili koje na nefiziološki način (privremeno) utiču na replikaciju. Rezultati ispitivanja genotoksičnosti obično se uzimaju kao indikatori mutagenih efekata.
3.5.2. Kriterijumi za klasifikaciju supstanci
3.5.2.1. U ovu klasu opasnosti klasifikuju se one supstance koje mogu da dovedu do mutacija germinativnih ćelija kod ljudi, a koje se mogu preneti na potomstvo. Pri klasifikaciji supstanci u ovu klasu opasnosti uzimaju u obzir i in vitro ispitivanja mutagenosti ili genotoksičnosti i in vivo ispitivanja na somatskim i germinativnim ćelijama sisara.
3.5.2.2. U postupku klasifikacije u odnosu na mutagenost germinativnih ćelija, supstance se klasifikuju unutar jedne od dve kategorije opasnosti ove klase opasnosti, kao što je prikazano u tabeli 3.5.1. koja je data u ovom prilogu.
Tabela 3.5.1. Kriterijumi za mutagenost germinativnih ćelija
Kategorija opasnosti |
Kriterijumi |
Kategorija 1 |
Supstance za koje se zna da dovode do naslednih mutacija ili za koje se smatra da dovode do naslednih mutacija germinativnih ćelija ljudi. |
Kategorija 1A |
Klasifikacija u kategoriju 1A zasniva se na pozitivnim podacima epidemioloških studija kod ljudi. |
Kategorija 1B |
Klasifikacija u kategoriju 1B zasniva se na: |
Kategorija 2 |
Supstance koje potencijalno mogu da izazovu nasledne mutacije germinativnih ćelija ljudi. |
3.5.2.3. Specifična razmatranja za klasifikaciju supstanci u odnosu na mutagenost germinativnih ćelija
3.5.2.3.1. U cilju klasifikacije razmatraju se rezultati dobijeni u eksperimentima za utvrđivanje mutegenih/genotoksičnih efekata na germinativne i/ili somatske ćelije kod životinja izloženih dejstvu te supstance. Uzimaju se u obzir i mutageni i/ili genotoksični efekti uočeni u in vitro ispitivanjima.
3.5.2.3.2. Klasifikacija se zasniva na opasnosti, pa se supstance klasifikuju na osnovu njihovog svojstva da mogu da izazovu mutacije germinativnih ćelija. Obrazac, stoga, ne obuhvata (kvantitativnu) procenu rizika koji ta supstanca predstavlja.
3.5.2.3.3. Klasifikacija na osnovu naslednih efekata na germinativne ćelije kod ljudi vrši se na osnovu rezultata ispitivanja koji su dobijeni propisanim metodama ispitivanja opasnih svojstava hemikalija ili drugim dobro sprovedenih validiranih ispitivanja. Rezultati ovih ispitivanja ocenjuju se na osnovu stručne procene. U cilju klasifikacije treba da bude procenjen i kvalitet svih dostupnih podataka.
3.5.2.3.4. U cilju klasifikacije razmatraju se rezultati in vivo ispitivanja nasledne mutagenosti germinativnih ćelija, kao što su:
- ispitivanja dominantno letalnih mutacija kod glodara i
- ispitivanja naslednih translokacija kod miša.
3.5.2.3.5. U cilju klasifikacije razmatraju se rezultati in vivo ispitivanja mutagenosti somatskih ćelija, kao što su:
- ispitivanja hromozomskih aberacija ćelija kostne srži sisara;
- spot test kod miša mikronukleus test na eritrocitima sisara.
3.5.2.3.6. U cilju klasifikacije razmatraju se rezultati ispitivanja mutagenosti, odnosno genotoksičnosti germinativnih ćelija, kao što su:
1) za ispitivanja mutagenosti:
- ispitivanja hromozomskih aberacija na spermatogonijama sisara;
- mikronukleus test kod spermatida,
2) za ispitivanja genotoksičnosti:
- test izmene sestrinskih hromatida kod spermatogonija;
- test neplanirane sinteze DNK (UDS) na ćelijama testisa.
3.5.2.3.7. U cilju klasifikacije razmatraju se rezultati ispitivanja genotoksičnosti kod somatskih ćelija, kao što su:
- in vivo test neplanirane sinteze DNK (UDS) na ćelijama jetre;
- test izmene sestrinskih hromatida (SCE) na ćelijama kostne srži.
3.5.2.3.8. U cilju klasifikacije razmatraju se rezultati in vitro ispitivanja mutagenosti, kao što su:
- in vitro ispitivanja hromozomskih aberacija kod sisara;
- in vitro ispitivanja genskih mutacija kod sisara;
- ispitivanja reverznih mutacija kod bakterija.
3.5.2.3.9. Klasifikacija pojedinačnih supstanci zasniva se na stručnoj proceni i utvrđivanju kvaliteta svih dostupnih podataka. U onim situacijama gde je za klasifikaciju korišćen jedan, dobro sproveden test, dobijeni rezultati se iskazuju jasno i nedvosmisleno. Nova, na odgovarajući način validirana ispitivanja mogu se takođe koristiti prilikom utvrđivanja ukupnog kvaliteta podataka za klasifikaciju. Potrebno je razmotriti i relevantnost puta izlaganja koji je korišćen u studiji u odnosu na put izlaganja ljudi.
3.5.3. Kriterijumi za klasifikaciju smeša
3.5.3.1. Klasifikacija smeša kada su dostupni podaci o svim sastojcima ili samo o nekim sastojcima smeše
3.5.3.1.1. Smešu treba klasifikovati kao smešu sa mutagenim svojstvima kada je najmanje jedan od njenih sastojaka klasifikovan u kategoriju 1A, 1B ili kategoriju 2 mutagenih supstanci i ako je u njoj prisutan u koncentraciji iznad opštih graničnih koncentracija koje su date u Tabeli 3.5.2. koja je data u ovom prilogu.
Tabela 3.5.2. Opšte granične koncentracije sastojaka smeše klasifikovanih kao mutageni germinativnih ćelija koje utiču na klasifikaciju te smeše
Sastojak koji je klasifikovan kao |
Granične koncentracije koje utiču na klasifikaciju smeše kao |
||
Kategorija 1A, mutagen |
Kategorija 1B, mutagen |
Kategorija 2, mutagen |
|
Kategorija 1A, mutagen |
≥ 0,1% |
- |
- |
Kategorija 1B, mutagen |
- |
≥ 0,1% |
- |
Kategorija 2, mutagen |
- |
- |
≥ 1,0% |
Napomena: Granične koncentracije navedene u ovoj tabeli odnose se na supstance u čvrstom i tečnom stanju (m/m), kao i na gasove (V/V).
3.5.3.2. Klasifikacija smeša kada su dostupni podaci o svojstvima same smeše
3.5.3.2.1. Klasifikacija smeša zasniva se na dostupnim eksperimentalnim podacima za pojedine sastojke smeše primenom graničnih koncentracija za sastojke koji su klasifikovani kao mutageni germinativnih ćelija. U pojedinim slučajevima, kada smeše pokazuju efekte koji nisu uočeni prilikom analize pojedinačnih sastojaka, podaci dobijeni ispitivanjem smeša mogu se koristiti za klasifikaciju. U takvim slučajevima, rezultati ispitivanja koji se odnose na smešu kao celinu prikazuju se na način da se na osnovu njih može jasno izvršiti klasifikacija, uzimajući u obzir dozu i ostale faktore kao što su: trajanje testa, period posmatranja, osetljivost i rezultati statističke analize pri ispitivanju mutagenosti germinativnih ćelija. Dokumentacija koja prati odluku o klasifikaciji čuva se i dostupna je radi eventualnog ponovnog razmatranja.
3.5.3.3. Klasifikacija smeša kada nisu dostupni podaci o svojstvima same smeše: Načela premošćavanja
3.5.3.3.1. Kada sama smeša nije ispitana radi utvrđivanja njene mutagenosti za germinativne ćelije, ali postoji dovoljno podataka o pojedinačnim sastojcima i sličnim smešama (u skladu sa odeljkom 3.5.3.2.1. ovog priloga) tako da je moguće na odgovarajući način okarakterisati opasnost smeše, ove podatke treba koristiti u skladu sa načelima premošćavanja datim u odeljku 1.1.3. ovog priloga.
3.5.4. Elementi obeležavanja
Elementi obeležavanja za supstance i smeše koje ispunjavaju uslove da budu klasifikovane u ovu klasu opasnosti dati su u Tabeli 3.5.3. koja je data u ovom prilogu.
Tabela 3.5.3. Elementi obeležavanja za mutagenost germinativnih ćelija
Klasifikacija |
Kategorija 1A/1B |
Kategorija 2 |
GHS piktogram opasnosti |
|
|
Reč upozorenja |
Opasnost |
Pažnja |
Obaveštenje o opasnosti |
H340: |
H341: |
Obaveštenja o merama predostrožnosti - prevencija |
P201 |
P201 |
Obaveštenja o merama predostrožnosti - reagovanje |
P308+P313 |
P308+P313 |
Obaveštenja o merama predostrožnosti - skladištenje |
P405 |
P405 |
Obaveštenja o merama predostrožnosti - odlaganje |
P501 |
P501 |
3.5.5. Dodatna razmatranja za klasifikaciju
Opšte je prihvaćeno da, u procesu tumorogeneze kod ljudi i životinja, hemikalije indukuju genetske promene, npr. protoonkogena i/ili tumorskih supresor gena somatskih ćelija. Shodno tome, supstance mutagene za somatske i/ ili germinativne ćelije in vivo mogu potencijalno biti i supstance sa karcinogenim svojstvom (videti odeljak 3.6.2.2.6. ovog priloga).
3.6.1. Definicija
Karcinogen je supstanca ili smeša koja dovodi do pojave karcinoma ili povećava incidencu njegove pojave. Za supstance koje su u dobro sprovedenim ispitivanjima na životinjama izazvale pojavu benignih ili malignih tumora pretpostavlja se ili sumnja da imaju karcinogeno dejstvo na ljude, osim ukoliko postoje dokazi da mehanizam nastajanja tumora nije od značaja za ljude.
3.6.2. Kriterijumi za klasifikaciju supstanci
3.6.2.1. Prilikom klasifikacije u odnosu na karcinogenost, supstance se klasifikuju u jednu od dve kategorije opasnosti na osnovu čvrstine dokaza i dodatnih razmatranja (kvaliteta podataka). U pojedinim slučajevima može biti opravdana klasifikacija za specifični put izlaganja, ukoliko se dokaže da drugi putevi izlaganja nisu od značaja.
Tabela 3.6.1. Kriterijumi za karcinogenost
Kategorija opasnosti |
Kriterijumi |
KATEGORIJA 1 |
Poznati karcinogen ili supstanca za koju se pretpostavlja da je karcinogena. |
Kategorija 1A |
Kategoriju 1A, supstance za koje je poznato da su karcinogene za ljude, klasifikacija je uglavnom bazirana na podacima koji se odnose na ljude; |
Kategorija 1B |
Kategoriju 1B, supstance za koje se pretpostavlja da su karcinogene za ljude, klasifikacija je uglavnom bazirana na podacima dobijenim u ispitivanjima na životinjama. Klasifikacija u kategorije 1A i 1B zasniva se na čvrstim dokazima i nekim dodatnim razmatranjima (videti odeljak 3.6.2.2. ovog priloga). Takvi dokazi mogu biti izvedeni iz: - studija o delovanju na ljude na osnovu kojih se može uspostaviti uzročno-posledična veza između izlaganja ljudi nekoj supstanci i razvoja karcinoma (poznati karcinogen za ljude) ili - eksperimenata na životinjama pri čemu postoji dovoljno* dokaza o karcinogenom delovanju na životinje (pa se pretpostavlja da je karcinogen i za ljude). Pored toga, prilikom razmatranja pojedinačnih slučajeva, ukoliko postoje ograničeni dokazi o karcinogenosti za ljude i ograničeni dokazi o karcinogenom delovanju na eksperimentalne životinje, na osnovu naučne procene može se opravdati klasifikacija supstance za koju se pretpostavlja da je karcinogena za ljude u kategoriju 1B. |
KATEGORIJA 2 |
Supstance za koje se sumnja da su karcinogene za ljude. |
Napomena*: videti odeljak 3.6.2.2.4. ovog priloga |
|
3.6.2.2. Posebna razmatranja za klasifikaciju supstanci kao karcinogenih
3.6.2.2.1. Klasifikacija supstance kao karcinogene vrši se na osnovu podataka dobijenih u pouzdanim, prihvaćenim metodama i predviđeno je da se primenjuje kod supstanci koje imaju svojstvo da izazovu karcinom. Procena se zasniva na svim dostupnim podacima, recenziranim publikovanim studijama i drugim prihvatljivim podacima.
3.6.2.2.2. Klasifikacija neke supstance kao karcinogene je postupak koji uključuje dve međuzavisne odrednice: procenu čvrstine dokaza i razmatranje svih drugih relevantnih podataka za klasifikaciju supstanci sa karcinogenim potencijalom za čoveka u odgovarajuću kategoriju opasnosti.
3.6.2.2.3. Čvrstina dokaza uključuje evidentiranje tumora kod ljudi i kod ispitivanih životinja i utvrđivanje stepena statističke značajnosti. Dovoljni dokazi o delovanju na ljude pokazuju uzročno-posledičnu vezu između izlaganja ljudi i razvoja karcinoma, dok dovoljni dokazi o delovanju na životinje ukazuju na uzročno-posledični odnos između supstance i povećane incidence tumora. Ograničeni dokazi o delovanju na ljude pokazuju da postoji pozitivna korelacija između izlaganja dejstvu neke supstance i karcinoma, ali bez uzročno-posledična veze. Ograničeni dokazi o delovanju na životinje su podaci koji ukazuju na karcinogeni efekat, ali nisu i dovoljni dokazi. Termini "dovoljan" i "ograničen" u ovom tekstu imaju značenje definisano od strane Međunarodne agencije za istraživanje karcinoma (International Agency for Reaserch on Cancer-IARC) i to:
1) Karcinogeno za ljude
Dokazi relevantni za karcinogenost, dobijeni u studijama kod ljudi, klasifikuju se u jednu od sledećih kategorija opasnosti:
- dovoljni dokazi za karcinogenost: ustanovljena uzročno-posledična veza između izlaganja i razvoja karcinoma kod ljudi. To podrazumeva da je pozitivna korelacija između izlaganja i pojave kancera dobijena u studijama u kojima se slučajnosti, bias i neusaglašeni rezultati mogu isključiti sa odgovarajućom pouzdanošću;
- ograničeni dokazi za karcinogenost: između izlaganja i pojave karcinoma postoji pozitivna veza, a interpretacija ove uzročno-posledične veze smatra se uverljivom, ali se slučajnosti, bias i neusaglašeni rezultati ne mogu isključiti sa dovoljnom pouzdanošću;
2) Karcinogeno za životinje
Karcinogenost kod eksperimentalnih životinja utvrđuje se primenom konvencionalnih metoda, metoda u kojima se koriste genetski modifikovane životinje i druge in vivo metode koje su zasnovane na jednom ili više kritičnih stadijuma karcinogeneze. U odsustvu podataka dobijenih u dugotrajnim konvencionalnim ispitivanjima ili ispitivanjima pojave neoplazija kao konačnog efekta, konzistentni pozitivni rezultati u nekoliko modela koji se odnose na različite stadijume višestepenog procesa karcinogeneze treba da budu razmatrani u proceni čvrstine dokaza za karcinogenost kod životinja. Dokazi relevantni za karcinogenost kod eksperimentalnih životinja klasifikuju se u jednu od sledećih kategorija opasnosti:
- dovoljni dokazi za karcinogenost: uzročno-posledična veza je ustanovljena između supstance i povećane incidence malignih neoplazmi kod (1) dve ili više vrsta eksperimentalnih životinja ili (2) dva ili više nezavisnih ispitivanja na jednoj vrsti eksperimentalnih životinja, sprovedenih u različitom vremenu ili u različitim laboratorijama ili primenom različitih protokola. Povećanje incidence tumora kod oba pola jedne vrste eksperimentalnih životinja, u dobro sprovedenom ispitivanju, sprovedenom po principima dobre laboratorijske prakse, može predstavljati dovoljan dokaz. Ukoliko se u pojedinačnoj studiji sprovedenoj na jednoj vrsti i polu, maligne neoplazme jave u neočekivanom stepenu u odnosu na incidencu, lokalizaciju, tip tumora ili starost životinje ili kada postoje jasni nalazi o većem broju mesta lokalizacije, ovakvo ispitivanje moglo bi biti razmatrano da se utvrdi da li obezbeđuje dovoljno dokaza;
- ograničeni dokazi za karcinogenost: podaci ukazuju na karcinogeno dejstvo ali su ograničeni pa se definitivan zaključak ne donosi zato što: (1) dokazi o karcinogenosti potiču iz samo jednog eksperimenta ili (2) postoje nerešena pitanja vezano za prihvatljivost eksperimentalnog dizajna ili interpretiranje ispitivanja ili (3) supstanca povećava incidencu samo benignih neoplazmi ili lezija sumnjivog neoplastičnog potencijala ili (4) dokazi o karcinogenosti potiču samo iz ispitivanja koja pokazuju isključivo promotornu aktivnost u ograničenom broju tkiva i organa.
3.6.2.2.4. Dodatna razmatranja (kao deo utvrđivanja kvaliteta podataka (videti odeljak 1.1.1. ovog priloga)). Pored procene čvrstine dokaza za karcinogenost, treba uzeti u obzir brojne druge faktore koji utiču na povećanje verovatnoće da neka supstanca bude karcinogena za ljude. Potpuna lista svih faktora bila bi veoma duga, ali su ovde razmotreni neki od važnijih faktora.
3.6.2.2.5. Ovi faktori mogu se posmatrati kao oni koji povećavaju ili smanjuju stepen zabrinutosti za karcinogenost kod ljudi. Relativni značaj koji će biti dat svakom faktoru zavisi od količine i koherentnosti dokaznog materijala svakog od njih pojedinačno. Uopšteno, postoji zahtev za kompletnijim podacima u cilju smanjenja, a ne povećanja zabrinutosti. U pojedinim slučajevima potrebna su dodatna razmatranja prilikom procene nalaza tumora i drugih faktora.
3.6.2.2.6. Neki važni faktori koji se mogu uzeti u razmatranje, kada se procenjuje stepen potencijalnog karcinogenog delovanja su:
1) tip tumora i postojeći podaci o incidenci;
2) više mesta lokalizacije;
3) progresija lezija u maligne oblike;
4) smanjeno latentno vreme pojave tumora;
5) da li do pojave tumora dolazi kod jednog ili oba pola;
6) da li do pojave tumora dolazi kod jedne ili više vrsta;
7) strukturna sličnost sa supstancom (supstancama) za koju postoje čvrsti dokazi o karcinogenom delovanju;
8) put izlaganja;
9) poređenje apsorpcije, distribucije, metabolizma i ekskrecije između eksperimentalnih životinja i ljudi;
10) mogućnost pojave neočekivanih efekata usled visoke toksičnosti primenjenih doza;
11) mehanizam delovanja i njegova relevantnost za ljude, kao što su citotoksičnost sa stimulacijom rasta, mitogeneza, imunosupresija, mutagenost.
Mutagenost: Poznato je da genetski procesi imaju centralnu ulogu u procesu razvoja karcinoma. Postojanje mutagene aktivnosti in vivo može da ukaže da neka supstanca ima karcinogeni potencijal.
3.6.2.2.7. Supstanca čija karcinogenost nije ispitana u određenim slučajevima može biti klasifikovana u kategorije 1A, 1B ili kategoriju 2 na osnovu podataka dobijenih za strukturno sličnu supstancu i razmatranjem drugih važnih faktora kao što je formiranje zajedničkih metabolita od značaja, npr. metaboliti kongenera benzidinskih boja.
3.6.2.2.8. Pri klasifikaciji se razmatra i da li se supstanca resorbuje datim putevima izlaganja ili da li se pojavljuju samo tumori lokalnog karaktera na mestima na kojima je ispitana supstanca primenjena, dok glavni putevi izlaganja ne dovode do karcinogenosti.
3.6.2.2.9. Važno je da se pri klasifikaciji uzmu u razmatranje sva saznanja koja se tiču fizičko-hemijskih, toksikokinetičkih i toksikodinamičkih svojstava supstance, kao svi dostupni relevantni podaci o hemijski sličnim supstancama, kao što su odnos njihove strukture i aktivnosti.
3.6.3. Kriterijumi za klasifikaciju smeša
3.6.3.1. Klasifikacija smeša kada su dostupni podaci o svim njenim sastojcima ili samo za pojedine sastojke smeše
3.6.3.1.1. Smešu se klasifikuje kao karcinogena kada je najmanje jedan od njenih sastojaka klasifikovan u kategoriju 1A ili 1B ili u kategoriji 2 karcinogenih supstanci i kada je prisutan u koncentraciji jednakoj ili većoj od odgovarajuće opšte granične koncentracije, kako je prikazano u Tabeli 3.6.2. koja je data u ovom prilogu.
Tabela 3.6.2. Opšte granične koncentracije sastojaka smeše klasifikovanih kao karcinogeni koja povlači klasifikaciju smeše
Sastojak klasifikovan kao |
Kategorija 1A, karcinogen |
Kategorija 1B, karcinogen |
Kategorija 2, karcinogen |
Kategorija 1A, karcinogen |
≥ 0,1% |
|
|
Kategorija 1B, karcinogen |
|
≥ 0,1% |
|
Kategorija 2, karcinogen |
- |
- |
≥ 1,0% |
Napomena: Granične koncentracije navedene u ovoj tabeli odnose se na supstance u čvrstom i tečnom stanju (m/m), ali i na gasove (V/V).
Napomena 1: Ukoliko je sastojak smeše koji je klasifikovan kao karcinogen kategorije 2 prisutan u koncentraciji ≥ 0,1%, bezbednosni list za smešu dostupan je na zahtev.
3.6.3.2. Klasifikacija smeša kada su dostupni podaci o svojstvima same smeše
3.6.3.2.1. Klasifikacija smeše zasniva se na dostupnim eksperimentalnim podacima dobijenim za pojedinačne sastojke smeše klasifikovane kao karcinogene primenom opštih graničnih koncentracija. U pojedinim slučajevima, za klasifikaciju se mogu koristiti podaci dobijeni ispitivanjem smeše ukoliko dobijeni efekti nisu uočeni kod pojedinačnih sastojaka. U takvim slučajevima, rezultati ispitivanja koji se odnose na smešu kao celinu prikazuju se tako da se na osnovu njih može izvršiti klasifikacija i to uzimajući u obzir dozu i druge faktore kao što su trajanje, period posmatranja, osetljivost i statistička analiza ispitivanja karcinogenosti. Dokumentacija na osnovu koje je izvršena klasifikacija treba da bude sačuvana i dostupna radi eventualne revizije na zahtev.
3.6.3.3. Klasifikacija smeša kada ne postoje podaci za pojedine sastojke smeše ili za samu smešu: Načela premošćavanja
3.6.3.3.1. Kada sama smeša nije ispitana radi utvrđivanja njene karcinogenosti, ali postoji dovoljno podataka o pojedinim sastojcima i sličnim smešama (videti odeljak 3.6.3.2.1. ovog priloga) tako da se stepen njene potencijalne opasnosti može odrediti, ove podatke treba koristiti u skladu sa načelima premošćavanja datim u odeljku 1.1.3. ovog priloga.
3.6.4. Elementi obeležavanja
Elementi obeležavanja za supstance i smeše koje ispunjavaju uslove da budu klasifikovane u ovu klasu opasnosti dati su u Tabeli 3.6.3. koja je data u ovom prilogu.
Tabela 3.6.3. Elementi obeležavanja za karcinogenost
Klasifikacija |
Kategorija 1A/1B |
Kategorija 2 |
GHS piktogram opasnosti |
|
|
Reč upozorenja |
Opasnost |
Pažnja |
Obaveštenje o opasnosti |
H350: |
H351: |
Obaveštenja o merama predostrožnosti - prevencija |
P201 |
P201 |
Obaveštenja o merama predostrožnosti - reagovanje |
P308+P313 |
P308+P313 |
Obaveštenja o merama predostrožnosti - skladištenje |
P405 |
P405 |
Obaveštenja o merama predostrožnosti - odlaganje |
P501 |
P501 |
3.7. Toksičnost po reprodukciju
3.7.1. Definicije i opšta uputstva
3.7.1.1. Toksičnost po reprodukciju predstavlja štetne efekte na seksualnu funkciju i plodnost kod odraslih jedinki muškog i ženskog pola, kao i razvojnu toksičnost kod potomstva. Dole navedene definicije preuzete su iz IPCS/EHC Dokumenta broj 225, Principi za procenu zdravstvenog rizika po reprodukciju izazvanog izlaganjem dejstvu hemikalija. Za potrebe ovog sistema klasifikacije smatra se da poznato izazivanje naslednih genetskih promena kod potomstva spada pod klasu opasnosti Mutagenost germinativnih ćelija (odeljak 3.5. ovog priloga).
Toksičnost po reprodukciju je podeljena na dva grupe efekata:
1) štetni efekti na seksualnu funkciju i plodnost;
2) štetni efekti na rast i razvoj potomstva.
Za pojedine toksične efekte na reprodukciju ne može se jasno utvrditi da li dovode do poremećaja seksualne funkcije i plodnosti ili rasta i razvoja potomstva. Ipak, supstance koje imaju navedene efekte ili smeše koje ih sadrže, biće klasifikovane kao toksične po reprodukciju sa opštim napomenama o njihovom toksičnom efektu.
3.7.1.2. Za potrebe klasifikacije, u okviru klase opasnosti Toksičnost po reprodukciju razlikuju se sledeći efekti:
1) štetni efekti na
- seksualnu funkciju i plodnost ili
- rast i razvoj;
2) efekti na ili preko laktacije.
3.7.1.3. Štetni efekti na seksualnu funkciju i plodnost
Ovi efekti predstavljaju dejstvo supstanci koje imaju potencijal da utiču na seksualnu funkciju i plodnost. Takav uticaj podrazumeva, ali nije ograničen na, poremećaje muškog i ženskog reproduktivnog sistema, štetne efekte na razvoj u pubertetu, proizvodnju i kretanje gameta, na normalan reproduktivni ciklus, seksualno ponašanje, plodnost, rađanje, ishod trudnoće, prerano reproduktivno sazrevanje ili modifikaciju ostalih funkcija koje zavise od integriteta reproduktivnog sistema.
3.7.1.4. Štetni efekti na rast i razvoj
Toksični efekti na rast i razvoj, u najširem smislu, obuhvataju sve efekte koji imaju uticaj na normalan razvoj ploda, bilo pre ili posle rođenja, a posledica su izlaganja roditelja dejstvu supstance pre začeća ili izlaganja potomstva u fazi razvoja pre ili posle rođenja, sve do perioda seksualne zrelosti. Smatra se da klasifikacija u odnosu na toksičnost po plod treba da upozori trudnice, kao i muškarce i žene u reproduktivnom periodu života. Toksičnost za razvoj se odnosi, pre svega, na štetne efekte tokom trudnoće ili na one koji su posledica izlaganja roditelja. Ova efekti mogu se ispoljiti u bilo kom trenutku života. Glavne posledice toksičnosti za rast i razvoj su: (1) smrt ploda, (2) strukturni poremećaji, (3) poremećaji rasta i (4) funkcionalni poremećaji.
3.7.1.5. Štetni efekti na ili preko laktacije su takođe uključeni u toksičnost po reprodukciju, ali su za svrhu klasifikacije ovi efekti posebno obrađeni u odeljak 3.7.2.1.2. ovog priloga. Supstance koje imaju štetno dejstvo na laktaciju posebno se klasifikuju, kako bi se dojilje upozorile na postojanje ove opasnosti preko posebnog obaveštenja.
3.7.2. Kriterijumi za klasifikaciju supstanci
3.7.2.1. Kategorije opasnosti
3.7.2.1.1. Za potrebe klasifikacije, u okviru klase opasnosti Toksičnost po reprodukciju, supstance se mogu klasifikovati u jednu od dve kategorije opasnosti. U okviru svake kategorije opasnosti odvojeno se razmatraju efekti na seksualnu funkciju i plodnost i efekti na rast i razvoj.
Tabela 3.7.1. Kriterijumi za toksičnost po reprodukciju
Kategorija opasnosti |
Kriterijumi* |
KATEGORIJA 1 |
Supstance za koje se zna ili se pretpostavlja da imaju toksične efekte na proces reprodukcije kod ljudi. |
Kategorija 1A |
Supstance za koje se zna da imaju toksične efekte na proces reprodukcije kod ljudi. |
Kategorija 1B |
Supstance za koje se pretpostavlja da imaju toksične efekte na proces reprodukcije kod ljudi. |
KATEGORIJA 2 |
Supstance za koje se sumnja da imaju toksične efekte na proces reprodukcije kod ljudi. |
Napomena*: Supstance koje svoje efekte ostvaruju na ili preko laktacije klasifikuju se u posebnu kategoriju opasnosti na osnovu kriterijuma koji su dati u odeljku 3.7.2.1.2. ovog priloga. |
|
3.7.2.1.2. Efekti na ili preko laktacije izdvojeni su u posebnu kategoriju opasnosti u okviru klase opasnosti Toksičnost po reprodukciju. Supstance koje svoje efekte ostvaruju na ili preko laktacije klasifikuju se u posebnu kategoriju opasnosti za efekte na ili preko laktacije. Kriterijumi za klasifikaciju u odnosu na efekte na ili preko laktacije su sledeći:
Supstance koje organizam žene apsorbuje, a koje mogu uticati na laktaciju ili se mogu izlučiti mlekom (uključujući i metabolite) u količinama koje predstavljaju rizik po odojčad, klasifikuju se i obeležavaju tako da se ukaže na opasnost po odojčad. Ove supstance se klasifikuju u odnosu na efekte na ili preko laktacije na osnovu:
1) dokaza kod ljudi koji ukazuju na opasnost po odojčad tokom perioda laktacije i/ili
2) rezultata studija sprovedenih na jednoj ili dve generacije životinja koji pružaju jasne dokaze da te supstance ostvaruju štetne efekte na potomstvo preko majčinog mleka ili da imaju štetne efekte na kvalitet mleka i/ili
3) ispitivanja absorpcije, metabolizma, distribucije i izlučivanja, a koja ukazuju da postoji verovatnoća da se takva supstanca nađe u majčinom mleku u toksičnim koncentracijama.
Napomena:. Uočeno je da za mnoge supstance ne postoje podaci o njihovom potencijalu da izazovu štetne efekte na potomstvo preko laktacije.
3.7.2.2. Osnove klasifikacije
3.7.2.2.1. Klasifikacija se vrši na osnovu odgovarajućih kriterijuma, gore navedenih, i procene kvaliteta podataka (odeljak 1.1.1. ovog priloga). Klasifikacija supstanci kao toksičnih po reprodukciju odnosi se na one supstance koje imaju specifično svojstvo da dovedu do štetnog efekta na reprodukciju, a ne na supstance koje takav efekat imaju samo kao nespecifičnu sekundarnu posledicu drugih toksičnih efekata.
Klasifikacija ovih supstanci vrši se u odgovarajuće kategorije opasnosti po sledećem redosledu: kategorija 1A, kategorija 1B, kategorija 2 i dodatna kategorija za efekte na i preko laktacije. Ukoliko supstanca zadovoljava kriterijume za klasifikaciju u obe glavne kategorije opasnosti (npr. kategorija 1B za efekte na seksualnu funkciju i plodnost i kategorija 2 za rast i razvoj) onda na etiketi treba da budu prikazana oba obaveštenja o opasnosti. Klasifikacija u dodatnu kategoriju za efekte na ili preko laktacije razmatra se bez obzira na klasifikaciju u kategoriju 1A, kategoriju 1B ili kategoriju 2.
3.7.2.2.2. Pri proceni toksičnih efekata na rast i razvoj potomstva potrebno je uzeti u obzir i toksičnost po majku (odeljak 3.7.2.4. ovog priloga)
3.7.2.2.3. Osnova za klasifikaciju u kategoriju 1A jeste pouzdan dokaz o štetnim efektima na reprodukciju ljudi. Najbolje bi bilo da dokazi na kojima se zasniva ovakva klasifikacija potiču iz dobro sprovedenih epidemioloških studija koje podrazumevaju odgovarajuću kontrolnu grupu, odgovarajuću procenu rezultata i procenu mogućih sistemskih grešaka (bias) ili dodatnih faktora (konfaundera).
Manje pouzdane podatke koji potiču iz zapažanja na ljudima treba zameniti odgovarajućim podacima iz ispitivanja na životinjama i razmotriti njihovu klasifikaciju u kategoriju 1B.
3.7.2.3. Utvrđivanje kvaliteta podataka
3.7.2.3.1. Klasifikacija supstanci kao toksičnih po reprodukciju vrši se na osnovu procene kvaliteta podataka (odeljak 1.1.1. ovog priloga). To znači da se svi dostupni podaci koji se odnose na toksičnost po reprodukciju razmatraju zajedno, kao što su epidemiološke studije, dobro dokumentovani prikazi slučajeva kod ljudi, specifična ispitivanja toksičnosti po reprodukciju na životinjama, zajedno sa rezultatima subhroničnih i hroničnih, kao i rezultatima specifičnih ispitivanja na životinjama koji obezbeđuju relevantne podatke o toksičnosti po reproduktivne i odgovarajuće endokrine organe. Ako su podaci o supstanci oskudni, potrebno je uzeti u obzir i podatke o hemijski sličnim supstancama. Na značaj podataka utiču različiti činioci, kao što su: kvalitet ispitivanja, konzistentnost rezultata, priroda i stepen efekata, postojanje eksperimentalnih dokaza na životinjama o toksičnosti po majku, nivo statističkog značaja za razlike između grupa, broja ciljnih pokazatelja na kojima je uočena promena, značaj ispitivanog puta izlaganja kod ljudi i postojanje grešaka (bias). I pozitivni i negativni rezultati se uzimaju u obzir pri proceni kvaliteta podataka. Samo jedna studija izvedena prema principima dobre naučne prakse sa statistički ili biološki značajnim pozitivnim rezultatima opravdava klasifikaciju (videti odeljak 3.7.2.2.3. ovog priloga).
3.7.2.3.2. Toksikokinetička ispitivanja na ljudima i životinjama, rezultati ispitivanja mesta i mehanizma ili načina dejstva supstance mogu da pruže relevantne podatke koji utiču na smanjenje ili povećanje zabrinutosti zbog njihove štetnosti po zdravlje ljudi. Ukoliko je u ovim ispitivanjima nedvosmisleno pokazano da mehanizam dejstva i put izlaganja supstance nisu relevantni za ljude ili ako su toksikokinetičke razlike takve da je sigurno da štetna svojstva supstance neće uticati na ljude, iako je u eksperimentalnim uslovima supstanca imala štetne efekte na životinjama, ovu supstancu ne treba klasifikovati.
3.7.2.3.3. Ukoliko se u pojedinim ispitivanjima toksičnosti po reprodukciju na eksperimentalnim životinjama pokaže da supstanca ima slabo toksično dejstvo, ne klasifikuju se obavezno. Ova dejstva uključuju manje promene u parametrima sperme ili pojavu spontanih poremećaja kod ploda, manje promene u proporcijama koje se uobičajeno prate kod ploda, a koje se, na primer, mogu primetiti prilikom pregleda skeleta, ili težine ploda ili u vidu manjih promena tokom rasta i razvoja posle rođenja.
3.7.2.3.4. Podaci dobijeni ispitivanjima na životinjama trebalo bi u idealnim uslovima da obezbede dokaze o specifičnom toksičnom delovanju na reprodukciju u odsustvu drugih sistemskih toksičnih efekata. Ipak, ukoliko se toksičnost za rast i razvoj pojavi zajedno sa drugim toksičnim dejstvima kod ženke, treba u što većoj meri proceniti moguća opšta toksična dejstva neke supstance. Najbolje je najpre razmotriti štetne efekte na embrion/fetus, a zatim proceniti toksične efekte na majku, zajedno sa drugim faktorima koji su mogli da utiču na pojavu takvih efekata, u sklopu utvrđivanja kvaliteta podataka o štetnosti neke supstance. Efekte na rast i razvoj koji se posmatraju pri primeni doza koje dovode do trovanja majke ne treba automatski odbaciti. Ovakva dejstva treba prihvatiti od slučaja do slučaja, u zavisnosti od toga da li je uzročno-posledična veza uspostavljena ili odbačena.
3.7.2.3.5. Ukoliko su na raspolaganju odgovarajući podaci, važno je odrediti da li je toksično delovanje supstance na rast i razvoj posledica specifičnog mehanizma prenosa toksičnosti sa intoksikovane majke na mladunce ili nespecifičnog, sekundarnog mehanizma, kao što je stres majke ili poremećaj homeostaze. Ukoliko se pouzdano utvrdi da su efekti na embrion/fetus posledica isključivo sekundarnih, nespecifičnih efekata, ovi podaci se ne uzimaju u obzir u postupku klasifikacije prema toksičnosti po majku. Ovo je naročito važno u slučajevima kada su uticaji na mladunce značajni, npr. ireverzibilni efekti kao što su strukturne malformacije. U pojedinim situacijama toksično delovanje supstance na proces reprodukcije se odbacuje zato što su toksični efekti posledica sekundarnih efekata toksičnosti po majku. Na primer, ukoliko je supstanca veoma toksična, kod ženke može doći do pojave takve iscrpljenosti da je ona nesposobna da odgaja i doji mladunce, pa oni ostaju bez hrane i umiru.
3.7.2.4. Toksičnost po majku
3.7.2.4.1. Tokom razvoja jedinke in utero i tokom rane faze postnatalnog razvoja mogu postojati toksični uticaji koji se prenose sa majke bilo kroz nespecifične mehanizme koji su povezani sa stresom i narušavanjem homeostaze u majčinom organizmu ili kroz specifične mehanizme kada intoksikovana majka prenosi toksičnost na svoje mladunce. Prilikom tumačenja uticaja supstance na rast i razvoj u cilju njene klasifikacije kao supstance koja remeti rast i razvoj treba uzeti u obzir i moguć uticaj toksičnosti po majku. Ovo je veoma složena odluka zbog neutvrđene veze između toksičnosti po majku i njenog uticaja na rast i razvoj. Stručna procena pri utvrđivanju kvaliteta podataka koji ukazuju na udeo toksičnosti po majku u toksičnom efektu neke supstance je ključna u klasifikaciji te supstance prema toksičnim efektima na rast i razvoj. Kako bi se došlo do pravilnih zaključaka o klasifikaciji supstance potrebno je najpre ispitati uticaj neke supstance na embrion/fetus, pa tek onda pristupiti ispitivanju posledica toksičnosti po majku, kao i ostalih činilaca koji su mogli imati uticaja na pojavu ovakvih efekata.
3.7.2.4.2. Na osnovu postojećih podataka, može se reći da toksičnost po majku, u zavisnosti od težine, utiče na razvoj ploda preko nespecifičnih, sekundarnih mehanizama i dovodi do pojave efekata kao što su smanjena težina fetusa, zakasnelo okoštavanje, moguća resorpcija i određene malformacije kod pojedinih vrsta životinja. Ograničen broj studija koje su sprovedene sa ciljem da se ustanovi veza između toksičnosti po majku i uticaja na razvoj ploda nisu uspele da pokažu doslednu, ponovljivu vezu kod određene vrste. Uticaji na rast i razvoj koji se javljaju u prisustvu toksičnosti po majku smatraju se jasnim dokazom toksičnog efekta supstance na rast i razvoj pre i posle rođenja, osim ukoliko se od slučaja do slučaja može dokazati da je uticaj na rast i razvoj sekundarna posledica toksičnosti po majku. Pored toga, klasifikacija supstance sprovodi se ukoliko su kod mladunaca primećeni značajni toksični efekti, npr. ireverzibilni efekti kao što su strukturne promene, smrt embriona/fetusa, značajni funkcionalni nedostaci posle rođenja.
3.7.2.4.3. Klasifikacija supstanci koje imaju štetan efekat na rast i razvoj samo preko toksičnosti po majku ne treba automatski da se prekine, čak iako je dokazan specifičan mehanizam kojim se toksičnost prenosi sa majke. U takvim slučajevima treba razmisliti o klasifikaciji takve supstance u kategoriju 2, pre nego u kategoriju 1. Kada je posledica toksičnog delovanja supstance smrt majke ili takva iscrpljenost da ona više ne može da doji svoje mladunce, onda toksični uticaj na postnatalni razvoj treba smatrati isključivo posledicom toksičnosti po majku i ovu supstancu ne treba klasifikovati kao supstancu sa toksičnim efektima na rast i razvoj ploda. Klasifikaciju supstance ne treba izvršiti u slučajevima manjih razvojnih promena kada se javljaju samo manje smanjenje težine fetusa/mladunaca ili zakasnelo okoštavanje koje je u tesnoj vezi sa toksičnošću po majku.
3.7.2.4.4. Podaci o pokazateljima za procenu toksičnosti po majku, ako su na raspolaganju, treba da budu procenjeni na osnovu njihove statističke ili biološke značajnosti kao i na osnovu odnosa doza-odgovor. Neki od pokazatelja za procenu toksičnosti po majku su:
- Smrtnost majki (povećana smrtnost među ispitivanim ženkama prestavlja dokaz o toksičnosti po majku ukoliko je ovo povećanje mortaliteta dozno zavisno i ako se može pripisati sistemskoj toksičnosti testirane supstance; smrtnost gravidnih ženki iznad 10% smatra se prekomernom i podatke za tu dozu ne bi trebalo uzimati u obzir za dalju procenu),
- Indeks parenja (br. polno zrelih mužjaka/broj sparenih životinja x 100),(16)
- Indeks plodnosti (br. oplođenih ženki/broj parenja x 100),
- Trajanje graviditeta (ukoliko je moguće izračunati),
- Telesna masa i promena telesne mase (podatke o promenama telesne mase i/ili promeni prilagođene telesne mase treba, kada takvi podaci postoje, uključiti u podatke koji se koriste za procenu toksičnih efekata neke supstance na majku. Izračunavanje prilagođene promene srednje vrednosti telesne mase kod ženke, koja predstavlja razliku između telesne mase pre graviditeta i telesne mase tokom graviditeta kada je nastupila promena, umanjena za težinu gravidne materice (sa plodom/plodovima može da pokaže da li je došlo do promene težine kod ženke ili njene materice; kod zečeva povećanje telesne težine nije pouzdan pokazatelj toksičnosti po majku jer su odstupanja u telesnoj težini tokom graviditeta kod zečeva uobičajena),
- Uzimanje vode i hrane, ukoliko je relevantno (praćenje da li postoji značajno povećanje u uzimanju hrane i vode kod ispitivanih ženki u odnosu na kontrolnu grupu može značajno uticati na procenu toksičnih efekata neke supstance po gravidne ženke, pogotovo kada se ispitivana supstanca daje preko hrane ili vode. Promene u količini hrane ili vode koja se unosi treba posmatrati u vezi sa promenama telesne mase gravidnih ženki kada se utvrđuje da li primećeni efekti predstavljaju posledicu intoksikacije ili ukusa ispitivanog materijala u hrani ili vodi.),
- Kliničke procene, uključujući kliničke znake, markere, hematološke i biohemijske nalaze (praćenje povećane učestalosti pojave značajnih kliničkih znakova trovanja kod ispitivanih ženki u odnosu na kontrolnu grupu je korisno kod procene toksičnih efekata neke supstance po majku. Ukoliko ovakva ispitivanja treba da predstavljaju osnovu za procenu toksičnosti za majku, onda se u studijama obavezno navode tipovi, učestalost, stepen i trajanje kliničkih znakova. Klinički znaci trovanja majki podrazumevaju: komu, iznemoglost, povećanu aktivnost, gubitak refleksa uspravljanja, prestanak pokretljivosti (ataksija) ili otežano disanje.),
- Post mortem podaci (povećana učestalost, odnosno ozbiljnost post mortem nalaza može biti pokazatelj trovanja gravidnih ženki. Oni mogu uključivati patoanatomske i patohistološke podatke ili podatke o težini organa, uključujući i apsolutnu težinu organa, odnos težine tela prema težini pojedinih organa ili odnos težine organa i težine mozga. Kada postoje i histopatološki nalazi zahvaćenih organa koji ukazuju na znatne promene tih organa kod ispitivanih gravidnih ženki u odnosu na kontrolnu grupu, to se smatra dokazom toksičnosti po majku).
________
(16) Smatra se da na vrednosti indeksa parenja i indeksa plodnosti mogu uticati i mužjaci.
3.7.2.5. Podaci dobijeni eksperimentalnim putem i ispitivanjem na životinjama
3.7.2.5.1. Postoje mnoge međunarodno priznate metode ispitivanja koje obuhvataju metode za ispitivanje toksičnosti po rast i razvoj (npr. OECD Uputstvo za ispitivanje 414) i metode za ispitivanje toksičnosti na jednoj ili dve generacije (npr. OECD Uputstvo za ispitivanje 415, 416).
3.7.2.5.2. Rezultati skrining testova (npr. OECD Uputstvo za ispitivanje 421 - skrining testovi toksičnosti po reprodukciju ili rast i razvoj i 422 - studije toksičnosti kombinovanim, ponovljenim dozama sa skrining testovima toksičnosti po reprodukciju kroz rast i razvoj) mogu takođe da se koriste za potvrdu klasifikacije, mada se rezultati ovakvih ispitivanja smatraju manje pouzdanim u odnosu na one koji su dobijeni potpunim ispitivanjem.
3.7.2.5.3. Štetni efekti ili promene, uočeni pri kratkotrajnim ili dugotrajnim ponavljanim dozama u ispitivanjima toksičnosti, za koje se proceni da remete reproduktivnu funkciju i koje se pojavljuju u odsustvu značajne opšte toksičnosti, mogu biti korišćeni kao osnova za klasifikaciju, npr. histopatološke promene na polnim žlezdama.
3.7.2.5.4. Klasifikaciji mogu doprineti dokazi dobijeni u in vitro testovima ili testovima na organizmima koji nisu sisari i izvedeni iz testova sa sličnim supstancama na osnovu veze strukture i aktivnosti (SAR). U svim ovakvim slučajevima, koristi se stručno mišljenje za procenu da li su podaci odgovarajući. Neodgovarajući podaci ne mogu se koristiti kao osnova za klasifikaciju.
3.7.2.5.5. Najbolje je da se u testovima na životinjama koriste odgovarajući putevi izlaganja supstanci koji imaju sličnosti sa mogućim putem izlaganja ljudi. U praksi, kada se određuje toksičnost po reprodukciju, obično se koristi peroralni unos i ovakva ispitivanja su obično pogodna za procenu rizika od toksičnog efekta na proces reprodukcije. Ukoliko ova ispitivanja nedvosmisleno pokazuju da se mehanizam i način dejstva supstance ne odnose na ljude ili ako su toksikokinetičke razlike tako jasne da je sigurno da se opasna svojstva supstance neće ispoljiti kod ljudi, iako je u eksperimentalnim uslovima takva supstanca pokazala štetne efekte na reprodukciju eksperimentalnih životinja, supstancu ne treba klasifikovati.
3.7.2.5.6. Ispitivanja u kojima se supstanca unosi intravenski ili intraperitonealno, što dovodi do izloženosti reproduktivnih organa nerealno visokim dozama ispitivane supstance, ili izaziva lokalna oštećenja ovih organa, uključujući i njihovu iritaciju, objašnjavaju se sa posebnim oprezom, a ovakva ispitivanja sama po sebi nisu osnova za klasifikaciju.
3.7.2.5.7. Postoji opšta saglasnost oko granične doze iznad koje se nastupanje štetnog efekta smatra da je van kriterijuma za klasifikaciju. U pojedinim uputstvima za izvođenje ispitivanja navedene su granične doze, dok se u drugim nailazi na preporuku da se po potrebi primene veće doze ako je očekivano izlaganje ljudi veće od odgovarajuće granice izloženosti. Pored toga, zahvaljujući toksikokinetičkim razlikama među vrstama, utvrđivanje specifičnih graničnih doza može biti neodgovarajuće u slučajevima kada su ljudi osetljiviji na efekte neke supstance od ispitivanih životinja.
3.7.2.5.8. Štetni efekti na proces reprodukcije koji se uočavaju samo kod primene visokih doza u ispitivanju na životinjama (uključujući i ona kod kojih dolazi do pojave iznemoglosti, težih oblika gubitka apetita, povećane smrtnosti) ne znače da će ta supstanca biti klasifikovana, osim ukoliko ne postoje i drugi podaci, npr. toksiko-kinetički koji upućuju na to da bi ljudi mogli biti podložniji njenom delovanju nego životinje, što bi ukazalo da je klasifikacija potrebna. Za dalja uputstva u ovoj oblasti pogledati odeljak 3.7.2.4. ovog priloga.
3.7.2.5.9. Da li će "granična doza" biti data ili ne zavisi od metode koja se koristi u ispitivanju, npr. u OECD Uputstvu za ispitivanje toksičnosti pri ponovljenom doziranju peroralno preporučuje se granična doza od 1000 mg/kg, osim u slučaju kada očekivani humani odgovor ukazuje da je potrebna veća doza.
3.7.3. Kriterijumi za klasifikaciju smeša
3.7.3.1. Klasifikacija smeše kada su dostupni podaci za sve ili samo za neke njene sastojke
3.7.3.1.1. Smeša se klasifikuje kao toksična po reprodukciju ako je najmanje jedan njen sastojak klasifikovan u kategoriju 1A ili 1B ili kategoriju 2 supstanci sa toksičnim efektom na reprodukciju i ako je taj sastojak smeše prisutan u koncentraciji iznad opšte granične koncentracije iz Tabele 3.7.2. koja je data u ovom prilogu za kategorije 1A ili 1B ili za kategoriju 2.
3.7.3.1.2. Smeša se klasifikuje kao ona koja toksičnost ispoljava na ili preko laktacije ukoliko je najmanje jedan njen sastojak tako klasifikovan, a prisutan je u smeši u koncentraciji iznad opšte granične koncentracije iz Tabele 3.7.2. za dodatnu kategoriju za efekte na ili preko laktacije.
Tabela 3.7.2. Opšte granične koncentracije sastojaka smeše koja su klasifikovani kao toksični po reprodukciju ili se njihovi toksični efekti ispoljavaju na ili preko laktacije što utiče na klasifikaciju smeše
Klasifikacija sastojka |
Opšte granične vrednosti koje utiču na klasifikaciju smeše |
|||
Kategorija 1A, toksičnost po reprodukciju |
Kategorija 1B, toksičnost po reprodukciju |
Kategorija 2, toksičnost po reprodukciju |
Dodatna kategorija za efekte na ili preko laktacije |
|
Kategorija 1A, toksičnost po reprodukciju |
≥ 0,3% |
|
|
|
Kategorija 1B, toksičnost po reprodukciju |
|
≥ 0,3% |
|
|
Kategorija 2, toksičnost po reprodukciju |
|
|
≥ 3,0% |
|
Dodatna kategorija za efekte na ili preko laktacije |
|
|
|
≥ 0,3% |
Napomena 1: Koncentracije navedene u ovoj tabeli odnose se na supstance u čvrstom i tečnom stanju (težinske jedinice), ali i na gasove (zapreminske jedinice).
Napomena 2: Ukoliko je sastojak iz smeše sa toksičnim dejstvom na reprodukciju iz kategorije 1 ili 2 prisutan u smeši u koncentraciji iznad 0,1%, bezbednosni list za smešu dostupan je na zahtev.
3.7.3.2. Klasifikacija smeše kada su dostupni podaci o svojstvima same smeše
3.7.3.2.1. U pojedinim slučajevima, za klasifikaciju se mogu koristiti podaci o smešama dobijeni u ispitivanjima kada one pokazuju efekte koji nisu uočeni prilikom ispitivanja pojedinačnih sastojaka. Rezultati ispitivanja koji se odnose na samu smešu kao celinu prikazuju se tako da je jasno da se na osnovu njih može izvršiti klasifikacija i to uzimajući u obzir dozu i druge faktore kao što su: trajanje, posmatranje, osetljivost i statistička analiza ispitivanja reproduktivnog sistema. Odgovarajuća dokumentacija koja prati odluku o klasifikaciji treba da bude sačuvana i dostupna u slučaju da je potrebna naknadna provera odluke.
3.7.3.3. Klasifikacija smeše kod kojih nisu dostupni podaci o svojstvima same smeše: Načela premošćavanja
3.7.3.3.1. U skladu sa odredbama odeljka 3.7.3.2.1, kada sama smeša nije ispitana radi utvrđivanja njene toksičnosti po reprodukciju, ali postoji dovoljno podataka koji se tiču pojedinačnih sastojaka i sličnih testiranih smeša tako da se stepen moguće opasnosti može pravilno odrediti, ove podatke treba koristiti na osnovu pravila za premošćavanje datih u odeljku 1.1.3. ovog priloga.
3.7.4. Elementi obeležavanja
Elementi obeležavanja za supstance i smeše koje ispunjavaju uslove da budu klasifikovane u ovu klasu opasnosti dati su u Tabeli 3.7.3. koja je data u ovom prilogu.
Tabela 3.7.3. Elementi obeležavanja za toksičnost po reprodukciju
Klasifikacija |
Kategorija 1A/1B |
Kategorija 2 |
Dodatno obeležavanje za supstance koje svoje štetno dejstvo ispoljavaju na ili preko laktacije |
GHS piktogram opasnosti |
|
|
Nema GHS |
Reč upozorenja |
Opasnost |
Pažnja |
Nema reči upozorenja |
Obaveštenje o opasnosti |
H360: |
H361: |
H362: |
Obaveštenja o merama predostrožnosti - prevencija |
P201 |
P201 |
P201 |
Obaveštenja o merama predostrožnosti - reagovanje |
P308+P313 |
P308+P313 |
P308+P313 |
Obaveštenja o merama predostrožnosti - skladištenje |
P405 |
P405 |
|
Obaveštenja o merama predostrožnosti - odlaganje |
P501 |
P501 |
|
3.8. Specifična toksičnost za ciljni organ - jednokratna izloženost
3.8.1. Definicija i opšta uputstva
3.8.1.1. Specifična toksičnost za ciljni organ - jednokratna izloženost predstavlja specifična, neletalna dejstva na pojedine organe posle jednokratne izloženosti supstanci ili smeši. Ovde spadaju sva značajna dejstva na zdravlje ljudi koja mogu da poremete normalno funkcionisanje nekog organa prolazno ili trajno, trenutno ili sa odloženim dejstvom, a nisu obrađeni u odeljcima 3.1. do 3.7. i odeljku 3.10. ovog priloga (videti odeljak 3.8.1.6. ovog priloga).
3.8.1.2. Klasifikacija supstanci ili smeša kao specifično toksičnih za ciljni organ (jednokratna izloženost) identifikuje ih kao specifično toksične za ciljni organ i kao potencijalno štetne po zdravlje ljudi koji su izloženi.
3.8.1.3. Ovi štetni efekti po zdravlje ljudi koji nastaju posle jednokratne izloženosti uključuju karakteristične toksične efekte na ljude ili toksikološki značajne promene funkcije ili morfologije tkiva/organa ili dovode do ozbiljnih promena biohemijskih ili hematoloških parametara kod eksperimentalnih životinja, koji su relevantni za zdravlje ljudi. Podaci o delovanju na ljude su najvažniji činioci za klasifikaciju.
3.8.1.4. Prilikom procene uzimaju se u obzir ne samo značajne promene u jednom organu ili biološkom sistemu, već i opšte promene manjeg intenziteta koje zahvataju više organa.
3.8.1.5. Specifična toksičnost za ciljni organ može se pojaviti nakon bilo kog puta izlaganja od značaja za ljude, npr. peroralno, dermalno ili inhalaciono.
3.8.1.6. Specifična toksičnost za ciljni organ - višekratna izloženost je obrađena u odeljku 3.9. ovog priloga, pa su takvi specifični toksični efekti izuzeti iz ovog odeljka. Ostali specifični toksični efekti nabrojani u daljem tekstu, obrađeni su posebno, pa su takođe izuzeti iz ovog odeljka:
1) akutna toksičnost (odeljak 3.1. ovog priloga);
2) korozivno oštećenje/iritacija kože (odeljak 3.2. ovog priloga);
3) teško oštećenje/iritacija oka (odeljak 3.3. ovog priloga);
4) senzibilizacija respiratornih organa ili kože (odeljak 3.4. ovog priloga);
5) mutagenost germinativnih ćelija (odeljak 3.5. ovog priloga);
6) kancerogenost (odeljak 3.6. ovog priloga);
7) toksičnost po reprodukciju (odeljak 3.7. ovog priloga) i
8) toksičnost posle aspiracije (odeljak 3.10. ovog priloga).
3.8.1.7. Klasa opasnih materija Specifična toksičnost za ciljni organ - jednokratna izloženost podeljena je na:
- specifičnu toksičnost za ciljni organ - jednokratna izloženost, kategorija 1 i 2;
- specifičnu toksičnost za ciljni organ - jednokratna izloženost, kategorija 3.
3.8.2. Kriterijumi za klasifikaciju supstanci
3.8.2.1. Klasifikacija supstance u kategoriju 1 i 2 specifične toksičnosti za ciljni organ (jednokratna izloženost)
3.8.2.1.1. Supstance sa trenutnim i odloženim dejstvom klasifikuju se u okviru različitih kategorija opasnosti na osnovu stručne procene i utvrđivanja kvaliteta podataka o dejstvu supstance, kao i preporučenih vrednosti (videti odeljak 3.8.2.1.9. ovog priloga). Supstance se klasifikuju u kategoriju 1 ili 2 u zavisnosti od njihove prirode i efekata koje izazivaju (Tabela 3.8.1. koja je data u ovom prilogu).
Tabela 3.8.1. Kriterijumi za specifičnu toksičnost za ciljni organ - jednokratna izloženost
Kategorija opasnosti |
Kriterijumi |
Kategorija 1 |
Supstance koje dovode do znatnih toksičnih efekata kod ljudi ili za koje se, na osnovu eksperimenata na životinjama, pretpostavlja da mogu da izazovu jake toksične efekte kod ljudi posle jednokratne izloženosti. |
Kategorija 2 |
Supstance za koje se na osnovu eksperimenata na životinjama može pretpostaviti da mogu imati štetno dejstvo na ljudsko zdravlje posle jednokratnog izlaganja. |
Kategorija 3 |
Prolazni efekti na ciljni organ. |
Napomena: Treba nastojati da se odredi primarni ciljni organ toksičnosti i u skladu sa tim klasifikovati, kao npr. supstance sa hepatotoksičnim dejstvom, sa neurotoksičnim dejstvom i slično. Treba pažljivo analizirati sve podatke i kad je moguće isključiti sekundarne efekte (supstance sa hepatotoksičnim dejstvom mogu imati sekundarne efekte na nervnom ili gastrointestinalnom sistemu).
3.8.2.1.2. Potrebno je odrediti i relevantan put izlaganja kojim klasifikovana supstanca ostvaruje svoja toksična dejstva.
3.8.2.1.3. Klasifikacija se vrši na osnovu stručne procene (odeljak 1.1.1. ovog priloga), utvrđivanjem kvaliteta svih podataka, uzimajući u obzir uputstva koja su data u daljem tekstu.
3.8.2.1.4. Kvalitet svih podataka (odeljak 1.1.1. ovog priloga), uključujući i incidente kod ljudi, epidemiološka, ispitivanja i ispitivanja na životinjama, služi da se potvrde specifični toksični efekti supstance za ciljni organ koji utiču na klasifikaciju.
3.8.2.1.5. Podaci potrebni za procenu specifične toksičnosti za ciljni organ mogu se odnositi na jednokratnu izloženost ljudi kod kuće, na radnom mestu ili u okruženju ili na istraživanja na životinjama. Standardna ispitivanja na životinjama izvode se na pacovima ili miševima i podrazumevaju ispitivanja akutne toksičnosti koje uključuju klinička posmatranja i detaljne makroskopske i mikroskopske preglede koji treba da otkriju toksično delovanje na ciljne organe ili tkiva ako oni postoje. Rezultati ispitivanja akutne toksičnosti sprovedene na drugim vrstama životinja takođe mogu obezbediti relevantne podatke.
3.8.2.1.6. U izuzetnim slučajevima, pojedine supstance sa specifičnom toksičnošću za ciljni organ mogu se klasifikovati u kategoriju 2, na osnovu stručne procene nalaza kod ljudi i to:
1) kada nalazi dobijeni kod ljudi nisu dovoljni da bi supstanca bila klasifikovana u kategoriju 1 i/ili
2) na osnovu prirode i intenziteta efekata.
Doze, odnosno koncentracije kod ljudi ne treba uzimati u obzir pri klasifikaciji i svi podaci dobijeni ispitivanjima na životinjama treba da budu u saglasnosti sa klasifikacijom u kategoriju 2. Ukoliko postoje podaci iz ispitivanja na životinjama koji ukazuju na klasifikaciju u kategoriju 1, supstancu treba klasifikovati u kategoriju 1.
3.8.2.1.7. Efekti koji se uzimaju u obzir za klasifikaciju u kategorije 1 i 2 specifične toksičnosti za ciljni organ (jednokratna izloženost).
3.8.2.1.7.1. Klasifikacija se vrši na osnovu podataka koji dovode u vezu jednokratnu izloženost supstanci sa očiglednim i karakterističnim toksičnim efektima.
3.8.2.1.7.2. Podaci o delovanju supstance na ljude dobijeni iz iskustva ili incidenata, obično su ograničeni na izveštaje o štetnim posledicama po zdravlje ljudi, često s nepouzdanim podacima o uslovima izloženosti i ne mogu da obezbede dovoljno naučnih podataka koji se mogu dobiti u dobro izvedenim ispitivanjima na životinjama.
3.8.2.1.7.3. Podaci dobijeni ispitivanjima na životinjama mogu pružiti mnogo više detalja u obliku kliničkih posmatranja, mikoroskopskih i makroskopskih patoloških pregleda, kada se često otkriju opasnosti od neke supstance, koje ne ugrožavaju život, ali koje mogu da ukažu na funkcionalni poremećaj. Svi raspoloživi podaci i relevantnost za ljudsko zdravlje uzimaju se u obzir prilikom klasifikacije, što podrazumeva i sledeće efekte na ljude i/ili životinje:
1) oboljevanje koje je posledica jednokratne izloženosti;
2) značajne funkcionalne promene respiratornog sistema koje nisu prolazne prirode, centralnog i perifernog nervnog sistema ili drugih organa ili organskih sistema, uključujući znake depresije centralnog nervnog sistema ili efekte na pojedina čula (kao što su čulo vida, sluha i mirisa);
3) svaka postojana i značajna promena biohemijskih ili hematoloških parametara ili promene uočene pri analizi mokraće;
4) znatna oštećenja organa koja su uočena pri patoanatomskom pregledu i/ili kasnije potvrđena mikroskopskim pregledom;
5) multifokalne ili difuzne nekroze, fibroze ili formiranja granuloma u vitalnim organima koji imaju sposobnost regeneracije;
6) morfološke promene koje su potencijalno reverzibilne, ali pružaju jasan dokaz o poremećaju funkcije organa;
7) dokazi o značajnom izumiranju ćelija (gde spada i degeneracija ćelija i smanjenje njihovog broja) kod vitalnih organa koji nemaju sposobnost regeneracije.
3.8.2.1.8. Efekti na osnovu kojih se ne može izvršiti klasifikacija supstance u kategorije 1 i 2 specifične toksičnosti za ciljni organ (jednokratna izloženost).
Ponekad se mogu uočiti efekti određenih supstanci koji ne opravdavaju njihovu klasifikaciju. Takvi efekti kod ljudi i/ili kod životinja između ostalog uključuju:
1) kliničko zapažanje ili male promene telesne mase, promene u unošenju hrane i vode, koji mogu imati toksikološki značaj, ali sami po sebi ne ukazuju na značajnu toksičnost;
2) manje promene u biohemijskim i hematološkim parametrima i promene uočene pri analizi mokraće i/ili prolazne efekte, kada su takve promene i efekti od sumnjivog ili minimalnog toksikološkog značaja;
3) promene u masi organa bez dokaza o poremećaju funkcije organa;
4) reakcije prilagođavanja za koje se ne smatra da su toksikološki bitne;
5) mehanizmi toksičnosti supstanci specifični za vrstu, tj. kada je sa sigurnošću dokazano da efekti nisu relevantni za ljude.
3.8.2.1.9. Preporučene vrednosti za klasifikaciju u kategorije 1 i 2 specifične toksičnosti za ciljni organ (jednokratna izloženost) na osnovu podataka iz ispitivanja na životinjama
3.8.2.1.9.1. Kako bi se olakšalo donošenje odluke o klasifikaciji supstance (u kategoriju 1 ili kategoriju 2 specifične toksičnosti za ciljni organ - jednokratna izloženost), određene su preporučene vrednosti koje se uzimaju u obzir za razmatranje doze, odnosno koncentracije supstance koja dovodi do značajnih uticaja na zdravlje. Osnovni razlog za uvođenje ovih preporučenih vrednosti je činjenica da sve supstance imaju moguće toksično dejstvo i da postoji određena doza/koncentracija iznad koje se njena toksičnost ispoljava.
3.8.2.1.9.2. Kada se u ispitivanjima na životinjama uoči toksično dejstvo koje je značajno za klasifikaciju, razmatranje doza, odnosno koncentracija pri kojima se to dejstvo ispoljilo u poređenju sa preporučenim vrednostima, obezbeđuje korisne podatke na osnovu kojih se odlučuje da li supstancu treba ili ne treba klasifikovati (jer su toksični efekti posledica štetnih svojstava same supstance, ali i njene doze/koncentracije).
3.8.2.1.9.3. Opseg preporučenih vrednosti (C) za izlaganje jednoj dozi koja je dovela do značajnog neletalnog toksičnog efekta je opseg koji se primenjuje za akutnu toksičnost, kao što je navedeno u Tabeli 3.8.2. koja je data u ovom prilogu.
Tabela 3.8.2. Opseg preporučenih vrednosti za specifičnu toksičnost za ciljni organ - jednokratna izloženost
|
|
Opseg preporučenih vrednosti za |
||
Put izlaganja |
Jedinice |
Kategorija 1 |
Kategorija 2 |
Kategorija 3 |
Peroralno (pacov) |
mg/kg telesne mase |
C ≤ 300 |
2000 ≥ C > 300 |
ne primenjuju se preporučene vrednosti |
Dermalno (pacov ili zec) |
mg/kg telesne mase |
C ≤ 1000 |
2000 ≥ C > 1000 |
|
Inhalacija gasa (pacov) |
ppmV/4h |
C ≤ 2500 |
5000 ≥ C > 2500 |
|
Inhalacija isparenja (pacov) |
mg/l/4h |
C ≤ 10 |
20 ≥ C > 10 |
|
Inhalacija prašine, magle, dima (pacov) |
mg/l/4h |
C ≤ 1,0 |
5,0 ≥ C > 1,0 |
|
Napomene:
1) Ove preporučene vrednosti i njihov opseg dati u Tabeli 3.8.2. treba samo da budu smernice, tj. da budu upotrebljene u okviru utvrđivanja kvaliteta podataka i da pomognu u donošenju odluke o klasifikaciji. One ne predstavljaju striktne vrednosti.
2) Ovakve vrednosti ne postoje za kategoriju 3 jer se klasifikacija vrši, pre svega, na osnovu podataka koji se odnose na ljude. Podaci koji potiču od ispitivanja na životinjama, ako postoje, treba da budu uključeni u postupak utvrđivanja kvaliteta podataka o delovanju neke supstance.
3.8.2.1.10. Dodatna uputstva
3.8.2.1.10.1. Kada je supstanca okarakterisana samo na osnovu podataka na životinjama (tipično za nove supstance, ali i za mnoge već poznate), proces klasifikacije podrazumeva upućivanje na preporučene doze, odnosno koncentracije kao važan elemenat za procenu kvaliteta podataka.
3.8.2.1.10.2. Kada postoje dobro potkrepljeni podaci o specifičnoj toksičnosti supstance za ciljni organ pri jednokratnoj izloženosti kod ljudi, takva supstanca treba da bude klasifikovana. Pozitivni podaci kod ljudi, bez obzira na doze, imaju veće vrednosti u smislu klasifikacije nego podaci dobijeni ispitivanjem na životinjama. Ako neka supstanca nije bila klasifikovana jer postojeći podaci nisu ukazivali na specifičnu toksičnost za ciljni organ kod ljudi, ali u međuvremenu postanu dostupni podaci iz incidenta koji ukazuju da ta supstanca ima specifičnu toksičnost za ciljni organ, onda ona treba da se klasifikuje.
3.8.2.1.10.3. Supstancu koja nije ispitana u smislu specifične toksičnosti za ciljni organ treba klasifikovati, ako je to moguće, na osnovu podataka o odnosu strukture i aktivnosti i na osnovu stručne procene podataka o strukturno sličnoj supstanci koja je ranije bila klasifikovana i na osnovu dodatnih činilaca, kao što je npr. formiranje zajedničkih, za toksičnost bitnih metabolita.
3.8.2.1.10.4. Koncentracije zasićenih isparenja takođe treba uvrstiti u elemente za klasifikaciju radi zaštite zdravlja ljudi i veće bezbednosti
3.8.2.2. Supstance iz kategorije 3: Prolazni efekti na ciljni organ
3.8.2.2.1. Kriterijumi za klasifikaciju supstance kao iritativne za respiratorne organe.
Kriterijumi za klasifikaciju supstanci u okviru kategorije 3 specifične toksičnosti za ciljni organ (jednokratna izloženost) kao iritativne za respiratorne organe su sledeći:
1) iritativni efekti na respiratorne organe (ograničeno crvenilo, edem, svrab i/ili bol), koji remete funkciju sa simptomima kao što su kašalj, bol, gušenje i smetnje disanja. Ova procena zasnovana je prvenstveno na podacima na ljudima;
2) subjektivno praćenje dejstva može biti podržano i merenjem iritacije respiratornog trakta (RTI) (kao što su elektrofiziološka reakcija, biomarkeri inflamacije u nazalnim ili bronhoalveolarnim sekretima);
3) simptomi uočeni kod ljudi treba da budu svojstveni široj populaciji izloženoj dejstvu neke supstance, a ne izolovane reakcije preosetljivosti ili odgovor izazvan samo kod pojedinaca sa preosetljivim disajnim putevima. Nedovoljno jasni izveštaji koji govore o "iritaciji" treba da budu odbačeni jer se ovi termini koriste za različite osećaje kao što su mirisi, neprijatan ukus, osećaj nadraženosti i suvoća, koji ne spadaju u tipične simptome iritacije respiratornih organa na osnovu kojih bi se izvršila klasifikacija;
4) u ovom trenutku ne postoje validirani testovi na životinjama koja mogu da mere iritaciju respiratornog trakta (RTI), međutim korisni podaci mogu se dobiti na osnovu jednokratnog ili ponovljenog ispitivanja inhalacione toksičnosti. Na primer, ispitivanje na životinjama može da obezbedi korisne podatke o kliničkim znacima toksičnosti (otežano disanje, rinitis itd.) i histopatološke podatke (npr. hiperemija, edem, minimalna inflamacija, zgusnuta sluz) koje su reverzibilne i mogu da budu odraz gore opisanih kliničkih simptoma. Ovakva ispitivanja na životinjama treba koristiti u proceni kvaliteta podataka;
5) ova klasifikacija je prikladna samo u slučaju kada nisu primećena ozbiljnija oštećenja organa, npr. respiratornog sistema.
3.8.2.2.2. Kriterijumi za klasifikaciju supstanci na osnovu narkotičkog dejstva.
Kriterijumi za klasifikaciju supstanci u okviru kategorije 3 na osnovu njenog narkotičkog dejstva su sledeći:
1) depresija centralnog nervnog sistema uključujući narkotičke efekte kod ljudi kao što su: pospanost, san, smanjena budnost, gubitak refleksa, nedostatak koordinacije i vrtoglavica. Ova dejstva mogu se manifestovati i kao jaka glavobolja ili mučnina i mogu dovesti do lošeg rasuđivanja, nesvestice, nervoze, umora, poremećaja pamćenja, poremećaja opažanja i koordinacije, poremećaja u vremenu reakcije ili pospanosti;
2) kod životinja simptomi narkotičkog dejstva supstance su letargija, loša koordinacija, gubitak refleksa uspravljanja i prestanak kretanja. Ukoliko ova dejstva nemaju prolazni karakter, supstancu koja ih je izazvala treba klasifikovati u kategoriju 1 ili 2 specifične toksičnosti za ciljne organe - jednokratna izloženost.
3.8.3. Kriterijumi za klasifikaciju smeša
3.8.3.1. Smeše se klasifikuju na osnovu istih kriterijuma koji važe i za supstance ili na način koji je opisan u daljem tekstu. Kao i supstance, smeše treba klasifikovati na osnovu specifične toksičnosti za ciljni organ posle jednokratne izloženosti.
3.8.3.2. Klasifikacija smeše kada su dostupni podaci o svojstvima same smeše
3.8.3.2.1. Kada su iz iskustva na ljudima ili iz odgovarajućih ispitivanja na životinjama dostupni pouzdani i kvalitetni podaci koji se odnose na smešu, kao što je opisano kod kriterijuma za klasifikaciju, onda se smeša klasifikuje na osnovu utvrđivanja kvaliteta ovih podataka (odeljak 1.1.1.4. ovog priloga). Posebnu pažnju treba obratiti na procenu podataka o smešama kako doze, trajanje, praćenje ili analize ne bi učinile takve rezultate neupotrebljivim.
3.8.3.3. Klasifikacija smeše kod kojih nisu dostupni podaci o svojstvima same smeše: Načela premošćavanja
3.8.3.3.1. Kada sama smeša nije ispitana radi utvrđivanja njene specifične toksičnosti za ciljni organ, ali ima dovoljno podataka o pojedinim sastojcima i sličnim već ispitanim smešama, da bi se opasnost od smeše mogla odgovarajuće okarakterisati, ovi se podaci koriste u skladu sa principima premošćavanja koji su opisani u odeljku 1.1.3. ovog priloga.
3.8.3.4. Klasifikacija smeše kada su dostupni podaci za sve ili samo za neke njene sastojke
3.8.3.4.1. Kada nema dovoljno pouzdanih dokaza ili podataka iz ispitivanja koja se odnose na samu smešu, a ni načela premošćavanja se ne mogu primeniti radi njene klasifikacije, onda se klasifikacija takvih smeša zasniva na klasifikaciji supstanci koje ulaze u njen sastav. Smešu treba klasifikovati kao smešu sa specifičnom toksičnošću za ciljni organ (navesti organ) posle jednokratne izloženosti, kada je barem jedan njen sastojak klasifikovan u kategoriju 1 ili 2 specifične toksičnosti za ciljni organ i prisutan je na nivou ili iznad opšte granične koncentracije date u Tabeli 3.8.3. koja je data u ovom prilogu za kategorije 1 i 2.
3.8.3.4.2. Opšte granične koncentracije i klasifikacija prikladno se primenjuju na jednokratnu izloženost supstanci sa specifičnom toksičnošću za ciljni organ.
3.8.3.4.3. Smeše treba nezavisno klasifikovati u jednu ili obe, jednokratnu i višekratnu toksičnost.
Tabela 3.8.3. Opšte granične koncentracije za sastojke smeše klasifikovane kao specifično toksične za ciljni organ, što utiče na klasifikaciju smeše u kategoriju 1 ili 2
Klasifikacija sastojka |
Opšte granične vrednosti koje utiču na klasifikaciju smeše |
|
Kategorija 1 |
Kategorija 2 |
|
Kategorija 1 |
koncentracija ≥ 10% |
1,0% ≤ koncentracija < 10% |
Kategorija 2 |
|
koncentracija ≥ 10% |
Napomena 1: Ukoliko je neki sastojak smeše sa specifičnom toksičnošću za ciljni organ iz kategorije 2 prisutan u smeši u koncentraciji iznad 1,0%, bezbednosni list za smešu dostupan je na zahtev.
3.8.3.4.4. Posebnu pažnju treba obratiti ako se u smeši nalaze toksični sastojci koji deluju na više od jednog sistema organa i treba uzeti u obzir njihovu potencijaciju ili sinergističke interakcije jer pojedine supstance mogu izazvati toksičnost za ciljni organ pri koncentraciji <1% kada neki drugi sastojak smeše pojačava njegovo toksično delovanje.
3.8.3.4.5. Posebnu pažnju treba obratiti pri ekstrapolaciji toksičnosti smeše koja sadrži sastojak iz kategorije 3. Odgovarajuća opšta granična koncentracija je 20%; ipak, ona može biti viša ili niža u zavisnosti od sastoj(a)ka iz kategorije 3 i toga da se neka dejstva, kao što je iritacija respiratornog trakta, možda neće pojaviti ispod određene koncentracije, dok se druga, kao što je narkotičko dejstvo, mogu pojaviti ispod ove vrednosti od 20%. U ovom slučaju potrebna je stručna procena.
Iritacija respiratornih organa i narkotički efekat posebno se ocenjuju u skladu sa kriterijumima navedenim u odeljku 3.8.2.2. ovog priloga. Kada se vrši klasifikacija za ove opasnosti, doprinos svakog sastojka smatra se aditivnim, osim ukoliko postoje dokazi da efekti nisu aditivni.
3.8.4. Elementi obeležavanja
Elementi obeležavanja za supstance i smeše koje ispunjavaju uslove da budu klasifikovane u ovu klasu opasnosti dati su u Tabeli 3.8.4. koja je data u ovom prilogu.
Tabela 3.8.4. Elementi obeležavanja za specifičnu toksičnost za ciljni organ nakon jednokratnog izlaganja
Klasifikacija |
Kategorija 1 |
Kategorija 2 |
Kategorija 3 |
GHS piktogram opasnosti |
|
|
|
Reč upozorenja |
Opasnost |
Pažnja |
Pažnja |
Obaveštenje o opasnosti |
H370: |
H371: |
H335: |
Obaveštenja o merama predostrožnosti - prevencija |
P260 |
P260 |
P261 |
Obaveštenja o merama predostrožnosti - reagovanje |
P307 + P311 |
P309 + P311 |
P304 + P340 |
Obaveštenja o merama predostrožnosti - skladištenje |
P405 |
P405 |
P403 + P233 |
Obaveštenja o merama predostrožnosti - odlaganje |
P501 |
P501 |
P501 |
3.9. Specifična toksičnost za ciljni organ - višekratna izloženost
3.9.1. Definicija i opšta uputstva
3.9.1.1. Specifična toksičnost za ciljni organ - višekratna izloženost predstavlja specifična dejstva na pojedine organe posle višekratne izloženosti supstanci ili smeši. Ovde spadaju sva značajna dejstva na zdravlje koja mogu da poremete normalno funkcionisanje nekog organa, prolazno i trajno, trenutno i/ili sa odloženim dejstvom, a koja nisu obrađena u odeljcima 3.1. do 3.8. i 3.10. ovog priloga.
3.9.1.2. Klasifikacija supstance ili smeše kao toksične za ciljni organ (višekratna izloženost) identifikuje je kao specifično toksičnu za ciljni organ i kao potencijalno štetnu po zdravlje ljudi koji su izloženi.
3.9.1.3. Ova štetni efekti po zdravlje obuhvataju toksične efekte na ljude ili eksperimentalne životinje, toksikološki značajne promene funkcije ili morfologije tkiva ili organa ili dovode do ozbiljnih promena biohemijskih ili hematoloških parametara kod eksperimentalnih životinja koji su relevantni za zdravlje ljudi.
3.9.1.4. Prilikom procene uzimaju se u obzir ne samo značajne promene u jednom organu ili biološkom sistemu, već i opšte promene manje teške prirode koje zahvataju više organa.
3.9.1.5. Specifična toksičnost za ciljni organ može može se pojaviti nakon bilo kog puta izlaganja od značaja za ljude, tj. peroralno, dermalno ili inhalaciono.
3.9.1.6. Neletalni toksični efekti na pojedine organe posle jednokratne izloženosti klasifikuju se kako je opisano za Specifičnu toksičnost za ciljni organ - jednokratna izloženost (odeljak 3.8. ovog priloga) i stoga su izuzeti iz ovog odeljka.
3.9.2. Kriterijumi za klasifikaciju supstanci
3.9.2.1. Supstance se klasifikuju u kategorije specifične toksičnosti za ciljni organ - višekratna izloženost na osnovu stručne procene i utvrđivanja kvaliteta podataka kao i preporučenih vrednosti koje uzimaju u obzir trajanje izloženosti i doze, odnosno koncentracije koja ima toksične efekte (videti odeljak 3.9.2.9. ovog priloga). Supstance se potom klasifikuju u kategoriju 1 ili 2 u zavisnosti od prirode i intenziteta efekata koje izazivaju (Tabela 3.9.1. koja je data u ovom prilogu).
Tabela 3.9.1. Kriterijumi za specifičnu toksičnost za ciljni organ - višekratna izloženost
Kategorija opasnosti |
Kriterijumi |
Kategorija 1 |
Supstance koje dovode do znatnih toksičnih efekata kod ljudi i za koje se na osnovu eksperimenata na životinjama predpostavlja da mogu da izazovu jake toksične efekte kod ljudi posle višekratne izloženosti. |
Kategorija 2 |
Supstance za koje se na osnovu eksperimenata na životinjama pretpostavlja da mogu imati štetne efekte na zdravlje ljudi posle višekratne izloženosti. |
Napomena: Nastoji se da se odredi primarni ciljni organ toksičnosti i u skladu sa tim klasifikovati, kao npr. supstance sa hepatotoksičnim dejstvom, sa neurotoksičnim dejstvom i slično. Pažljivo se analiziraju svi podaci i, kad je to moguće, isključuju sekundarni efekti (supstance sa hepatotoksičnim dejstvom mogu imati sekundarne efekte na nervnom ili gastrointestinalnom sistemu).
3.9.2.2. Treba odrediti bitan put izlaganja kojim klasifikovana supstanca izaziva svoja toksična dejstva.
3.9.2.3. Klasifikacija se vrši na osnovu stručne procene (odeljak 1.1.1. ovog priloga), na osnovu kvaliteta svih podataka uključujući i uputstvo za klasifikaciju dato u odeljku 3.9.2.4. ovog priloga.
3.9.2.4. Kvalitet svih podataka (odeljak 1.1.1. ovog priloga), uključujući i incidente kod ljudi, epidemiološka i ispitivanja na životinjama, služi da se potvrde specifični toksični efekti supstance za ciljni organ koji su bitni za klasifikaciju. Koriste se i podaci iz oblasti industrijske toksikologije sakupljani tokom godina. Procena se bazira na svim postojećim podacima, uključujući objavljene studije i dodatne prihvatljive podatke.
3.9.2.5. Podaci potrebni za procenu specifične toksičnosti za ciljni organ dobijaju se ili iz višekratne izloženosti ljudi kod kuće, na radnom mestu ili u okruženju ili iz ispitivanja na životinjama. Standardna ispitivanja na pacovima ili miševima koja obezbeđuju ove podatke traju 28 ili 90 dana ili tokom njihovog životnog ciklusa (do dve godine) i uključuju hematološka, kliničko-biohemijska i detaljne makroskopske i mikroskopske preglede u cilju određivanja toksičnih efekata na ciljna tkiva/organe. Rezultati ispitivanja posle ponovljenog doziranja na drugim životinjskim vrstama takođe mogu obezbediti relevantne podatke. I druga ispitivanja posle dugotrajne izloženosti, kao što su ispitivanja karcinogenosti, neurotoksičnosti ili toksičnosti po reprodukciju, mogu takođe obezbediti podatke o specifičnoj toksičnosti za ciljni organ koji bi se mogli koristiti u proceni za klasifikaciju.
3.9.2.6. U izuzetnim slučajevima, na osnovu stručne procene, pojedine supstance sa specifičnom toksičnošću za ciljni organ, na osnovu nalaza kod ljudi, mogu se klasifikovati u kategoriju 2:
1) kada nalazi dobijeni kod ljudi nisu dovoljni da bi supstanca bila klasifikovana u kategoriju 1 i/ili
2) na osnovu prirode i intenziteta efekata.
Doze, odnosno koncentracije kod ljudi ne treba uzimati u obzir pri klasifikaciji i svi podaci dobijeni u ispitivanjima na životinjama treba da budu odgovarajući za klasifikaciju u kategoriju 2. Ako neki od podataka iz ispitivanja na životinjama ukazuju da je odgovarajuća klasifikacija u kategoriju 1, supstancu treba klasifikovati u kategoriju 1.
3.9.2.7. Efekti koji se uzimaju u obzir u postupku klasifikacije u kategorije specifične toksičnosti za ciljni organ - višekratna izloženost.
3.9.2.7.1. Klasifikacija supstanci vrši se na osnovu pouzdanih podataka koji dovode u vezu višekratnu izloženost sa očiglednim i karakterističnim toksičnim efektima supstance.
3.9.2.7.2. Podaci o delovanju supstance na ljude dobijeni iz iskustva ili incidenata, obično su ograničeni na izveštaje o štetnim posledicama po zdravlje ljudi, često su nepouzdani u pogledu o uslova izloženosti i ne obezbeđuju dovoljno naučnih podataka koji se dobijaju dobro izvedenim ispitivanjima na životinjama.
3.9.2.7.3. Podaci dobijeni u ispitivanjima na životinjama mogu pružiti mnogo više detalja, u vidu kliničkih posmatranja, hematoloških, kliničko-biohemijsih, mikroskopskih i makroskopskih patoloških pregleda u kojima se često identifikuju opasnosti od neke supstance, koje ne ugrožavaju život, ali koje mogu da ukažu na funkcionalni poremećaj. Svi raspoloživi podaci i relevantnost za ljudsko zdravlje uzimaju se u obzir prilikom klasifikacije uključujući, između ostalih, i sledeće efekte na ljude i/ili životinje:
1) oboljevanje ili smrt kao posledica višekratne ili dugotrajne izloženosti. Oboljevanje ili smrt može biti rezultat višekratne izloženosti, čak i relativno niskim dozama, odnosno koncentracijama, usled bioakumulacije supstance ili njenih metabolita, odnosno zbog zasićenja procesa detoksikacije usled ponovljene izloženosti supstanci ili njenim metabolitima;
2) značajne funkcionalne promene u centralnom ili perifernom nervnom sistemu ili drugim sistemima organa, uključujući znake depresije centralnog nervnog sistema i efekte na posebna čula (kao što su čulo vida, sluha i mirisa);
3) svaka postojana i značajna promena kliničko-biohemijskih, hematoloških ili parametara analize mokraće;
4) znatno oštećenje organa uočeno pri patoanatomskom pregledu i/ili kasnije potvrđeno mikroskopskim pregledom;
5) multifokalna ili difuzna nekroza, fibroza ili formiranje granuloma u vitalnim organima koji imaju sposobnost regeneracije;
6) morfološke promene koje su potencijalno reverzibilne, ali pružaju jasan dokaz o poremećaju funkcije organa (npr. teška masna degeneracija jetre);
7) dokazi o značajnom izumiranju ćelija (uključujući degeneraciju ćelija i smanjenje njihovog broja) kod vitalnih organa koji nemaju sposobnost regeneracije.
3.9.2.8. Efekti na osnovu kojih se ne može izvršiti klasifikacija supstance u kategorije 1 i 2 specifične toksičnosti za ciljni organ posle višekratne izloženosti:
3.9.2.8.1. Ponekad se mogu uočiti efekti određenih supstanci kod ljudi ili životinja koji ne opravdavaju klasifikaciju. Takvi efekti uključuju i:
1) kliničko zapažanje ili neznatne promene u povećanju telesne mase, promene u unosu hrane ili vode, koji imaju toksikološki značaj ali sami po sebi ne ukazuju na "značajnu" toksičnost;
2) neznatne promene u kliničko-biohemijskim, hematološkim ili parametrima analize mokraće, odnosno prolazni efekti, kada su takve promene i efekti od sumnjivog ili minimalnog toksikološkog značaja;
3) promene u masi organa bez dokaza o poremećaju funkcije organa;
4) reakcije prilagođavanja za koje se ne smatra da su toksikološki bitne;
5) mehanizme toksičnosti supstanci koji su specifični za vrstu, tj. kada je sa sigurnošću dokazano da efekti nisu relevantni za ljude, onda klasifikacija nije opravdana.
3.9.2.9. Preporučene vrednosti za klasifikaciju u kategorije 1 i 2 specifične toksičnosti za ciljni organ (višekratna izloženost) na osnovu podataka iz ispitivanja na životinjama
3.9.2.9.1. U ispitivanjima na životinjama, nemoguće je osloniti se samo na posmatranje efekata bez podataka o dužini izloženosti tokom eksperimenta i doze/koncentracije, jer se time izuzimaju osnovne postavke toksikologije, tj. sve supstance mogu da budu toksične, a doza/koncentracija i dužina izlaganja su činioci koji određuju toksičnost. U većini eksperimenata na životinjama koriste se gornje granične vrednosti doza.
3.9.2.9.2. Da bi se olakšalo donošenje odluke da li treba klasifikovati supstancu i u koju kategoriju (kategorija 1 ili kategorija 2), date su preporučene vrednosti doze, odnosno koncentracije supstance radi razmatranja doza/koncentracija za koje je pokazano da značajno utiču na zdravlje.
Osnovni razlog za uvođenje ovih preporučenih vrednosti je činjenica da sve supstance mogu biti toksične i da postoji određena doza/koncentracija iznad koje se toksičnost ispoljava.
Ispitivanja na životinjama primenom ponovljenih doza namenjena su da izazovu toksične efekte kako bi se postigao cilj ovih ispitivanja i da većina studija otkrije neko toksično dejstvo supstance bar pri primeni najviših doza. Ne odlučuje se samo kakve efekte supstanca može da izazove, već i na kojim nivoima doza/koncentracija i koliko su ovi efekti relevantni za ljude.
3.9.2.9.3. Kada se u ispitivanjima na životinjama uoči značajno toksično dejstvo koje zahteva klasifikaciju, razmatranje dužine izloženosti u eksperimentu i doza, odnosno koncentracija pri kojima su ta dejstva uočena u poređenju sa preporučenim vrednostima obezbeđuje korisne podatke na osnovu kojih se može doneti odluka da li supstancu treba ili ne treba klasifikovati (jer su toksični efekti posledica štetnih svojstava same supstance, ali i dužine izloženosti i doze, odnosno koncentracije).
3.9.2.9.4. Na odluku da li neku supstancu treba klasifikovati može uticati i podatak o preporučenoj dozi, odnosno koncentraciji pri kojoj ili ispod koje se ne uočava značajno toksično dejstvo.
3.9.2.9.5. Ove preporučene vrednosti odnose se na dejstva koja su zapažena pri standardnim 90-to dnevnim studijama toksičnosti sprovedenim na pacovima. Ove vrednosti mogu poslužiti kao osnova za izvođenje odgovarajućih preporučenih vrednosti u studijama toksičnosti za dužu ili kraću izloženost, ekstrapolacijom vremena izloženosti u dozu slično Haberovom pravilu o inhalaciji po kome je doza sa efektom direktno proporcionalna koncentraciji supstance i dužini izloženosti. Procenu treba vršiti od slučaja do slučaja, npr. vrednosti za 28-dnevne studije dobiće se tako što se preporučene vrednosti pomnože faktorom tri.
3.9.2.9.6. Stoga se klasifikacija u kategoriju 1 primenjuje kada se značajni toksični efekti, uočeni posle višekratne izloženosti u 90-dnevnoj studiji sprovedenoj na eksperimentalnim životinjama, pojavljuju na nivou ili ispod preporučenih vrednosti koje su date u Tabeli 3.9.2. koja je data u ovom prilogu.
Tabela 3.9.2. Preporučene vrednosti za klasifikaciju supstanci u kategoriju 1 specifične toksičnosti za ciljni organ - višekratna izloženost
Put izlaganja |
Jedinice |
Preporučene vrednosti (doza/koncentracija) |
Peroralno (pacov) |
mg/kg t.m. |
C ≤ 10 |
Dermalno (pacov ili zec) |
mg/kg t.m. |
C ≤ 20 |
Inhalaciono (pacov) gas |
ppmV/6h/dan |
C ≤ 50 |
Inhalaciono (pacov) pare |
mg/l/6h/dan |
C ≤ 0,2 |
Inhalaciono (pacov) prašina/magla/dim |
mg/l/6h/dan |
C ≤ 0,02 |
3.9.2.9.7. Klasifikacija u kategoriju 2 se primenjuje kada se značajni toksični efekti uočeni posle višekratne izloženosti u 90-dnevnoj studiji sprovedenoj na eksperimentalnim životinjama, javljaju u opsegu preporučenih vrednosti koje su date u Tabeli 3.9.3. koja je data u ovom prilogu.
Tabela 3.9.3. Preporučene vrednosti koje treba da pomognu klasifikaciju supstanci u kategoriju 2
Put izlaganja |
Jedinice |
Opseg preporučenih vrednosti (doza/koncentracija) |
Peroralno (pacov) |
mg/kg t.m. /dan |
10 < C ≤ 100 |
Dermalno (pacov ili zec) |
mg/kg t.m. /dan |
20 < C ≤ 200 |
Inhalaciono (pacov) gasa |
ppmV/6h/dan |
50 < C ≤ 250 |
Inhalaciono (pacov) pare |
mg/l/6h/dan |
0,2 < C ≤ 1,0 |
Inhalaciono (pacov) prašine/magle/dima |
mg/l/6h/dan |
0,02 < C ≤ 0,2 |
3.9.2.9.8. Navedene preporučene vrednosti i opsezi vrednosti dati u odeljcima 3.9.2.9.6. i 3.9.2.9.7. ovog priloga predstavljaju samo smernice, tj. upotrebljavaju se za utvrđivanje kvaliteta podataka i pomažu u donošenju odluke o klasifikaciji. Oni ne predstavljaju striktne vrednosti.
3.9.2.9.9. Moguće je da se specifični profil toksičnosti pojavi u studijama na životinjama, ponovljena izloženost, pri dozama/koncentracijama koje su ispod navedenih preporučenih vrednosti, npr. ispod 100 mg/kg telesne mase po danu (t.m./dan) pri peroralnom unosu, međutim priroda efekta (npr. nefrotoksičnost) je takva da se javlja samo kod mužjaka pacova određene vrste za koje se zna da su osetljivi prema tom efektu, pa se supstanca ne mora klasifikovati. I obratno, moguće je da se specifični profil toksičnosti pojavi u studijama na životinjama pri dozama koje su iznad preporučenih, kao npr. ≥ 100 mg/kg t.m./dan pri peroralnom unosu, a postoje i dodatni podaci iz drugih izvora, kao što su ispitivanja dugotrajne primene supstance ili iskustva kod ljudi, koje podržavaju odluku sa stanovišta utvrđivanja kvaliteta podataka da je klasifikacija potrebna.
3.9.2.10. Dodatna uputstva
3.9.2.10.1. Kada je supstanca okarakterisana samo na osnovu podataka na životinjama (tipično za nove supstance, ali i za mnoge već poznate), proces klasifikacije podrazumeva upućivanje na preporučene doze, odnosno koncentracije kao važan elemenat za procenu kvaliteta podataka.
3.9.2.10.2. Supstancu treba klasifikovati kada postoje dobro potkrepljeni podaci o specifičnoj toksičnosti supstance za ciljni organ kod ljudi, koja se pripisuje ponovljenom ili dugotrajnom izlaganju. Pozitivni rezultati dobijeni kod ljudi, bez obzira na dozu, značajniji su od podataka dobijenih ispitivanjem na životinjama. Ako neka supstanca nije klasifikovana jer nije uočena specifična toksičnost za ciljni organ na nivou ili ispod preporučenih doza, odnosno koncentracija za ispitivanje na životinjama, a kasniji podaci o incidentu kod ljudi ukazuju da ta supstanca ima specifičnu toksičnost za ciljni organ, onda je treba klasifikovati.
3.9.2.10.3. Supstancu koja nije ispitana u smislu specifične toksičnosti za ciljni organ, treba klasifikovati, ako je to moguće, na osnovu podataka o vezi strukture i aktivnosti i na osnovu stručne procene podataka o strukturno sličnim supstancama koje su prethodno klasifikovane i na osnovu dodatnih činilaca, kao što je npr. formiranje zajedničkih za toksičnost bitnih metabolita.
3.9.2.10.4. Koncentracije zasićenih isparenja takođe treba uvrstiti u elemente za klasifikaciju radi zaštite zdravlje i veće sigurnosti.
3.9.3. Kriterijumi za klasifikaciju smeša
3.9.3.1. Smeše se klasifikuju na osnovu istih kriterijuma koji važe i za supstance ili na način koji je opisan u daljem tekstu. Kao i supstance, smeše treba klasifikovati na osnovu specifične toksičnosti za ciljni organ posle višekratne izloženosti.
3.9.3.2. Klasifikacija smeše kada su dostupni podaci o svojstvima same smeše
3.9.3.2.1. Kada su dostupni pouzdani i kvalitetni podaci kod ljudi ili iz odgovarajućih ispitivanja na životinjama, kao što je opisano kod kriterijuma za klasifikaciju supstanci, a koji se odnose na samu smešu (odeljak 1.1.1.4. ovog priloga), onda se smeša klasifikuje na osnovu utvrđivanja kvaliteta ovih podataka. Posebnu pažnju treba obratiti na procenu podataka o smešama kako doza, trajanju, praćenje ili analiza ne bi učinile rezultate neupotrebljivim za zaključivanje o klasifikaciji.
3.9.3.3. Klasifikacija smeše kada nisu dostupni podaci o svojstvima same smeše: Načela premošćavanja
3.9.3.3.1. Kada sama smeša nije ispitana radi utvrđivanja njene specifične toksičnosti za ciljni organ, ali ima dovoljno podataka o pojedinim sastojcima i sličnim, već ispitanim smešama da bi se opasnost od smeše mogla odgovarajuće proceniti, ovi podaci koriste se u skladu sa načelima premošćavanja koja su opisana u odeljku 1.1.3. ovog priloga.
3.9.3.4. Klasifikacija smeše kada su dostupni podaci za sve ili samo za neke njene sastojke
3.9.3.4.1. Kada nema pouzdanih dokaza ili podataka iz ispitivanja koji se odnose na samu smešu, a ni načela premošćavanja ne mogu da se primene za klasifikaciju, onda se klasifikacija takvih smeša zasniva na klasifikaciji supstanci koje ulaze u njen sastav. Smešu treba klasifikovati kao smešu sa specifičnom toksičnošću za ciljni organ (navesti organ), posle jednokratne ili višekratne izloženosti ili posle obe, kada je bar jedan njen sastojak klasifikovan u kategoriju 1 ili 2 specifične toksičnosti za ciljni organ i nalazi se na nivou ili iznad odgovarajućih opštih graničnih koncentracija datih u Tabeli 3.9.4. koja je data u ovom prilogu.
Tabela 3.9.4. Opšte granične koncentracije za sastojke smeše klasifikovane kao specifično toksične za ciljni organ, što utiče na klasifikaciju smeše
Klasifikacija sastojka |
Opšte granične vrednosti koje utiču na klasifikaciju smeše |
|
Kategorija 1 |
Kategorija 2 |
|
Kategorija 1 |
koncentracija ≥ 10% |
1,0% ≤ koncentracija < 10% |
Kategorija 2 |
|
koncentracija ≥ 10% |
Napomena 1: Ukoliko je neki sastojak smeše sa specifičnom toksičnošću za ciljni organ iz kategorije 2 prisutan u smeši u koncentraciji ≥ 1,0%, bezbednosni list za smešu dostupan je na zahtev.
3.9.3.4.2. Opšte granične koncentracije i odgovarajuću klasifikaciju treba primeniti u slučaju toksikanata sa specifičnom toksičnošću za ciljni organ pri višekratnom izlaganju.
3.9.3.4.3. Nezavisno se razmatra klasifikacija smeše u odnosu na toksičnost posle jednokratnog i u odnosu na toksičnost posle višekratnog izlaganja.
3.9.3.4.4. Posebnu pažnju treba obratiti u slučaju kada se u smeši nalaze toksikanti koji deluju na više od jednog sistema organa kada treba uzeti u obzir njihovu potencijaciju ili sinergističke interakcije jer pojedine supstance mogu izazvati toksičnost za ciljni organ pri koncentraciji <1% kada neki drugi sastojak smeše pojačava njegovo toksično delovanje.
3.9.4. Elementi obeležavanja
Elementi obeležavanja za supstance i smeše koje ispunjavaju uslove da budu klasifikovane u ovu klasu opasnosti dati su u Tabeli 3.9.5. koja je data u ovom prilogu.
Tabela 3.9.5. Elementi obeležavanja za specifičnu toksičnost za ciljni organ nakon višekratnog izlaganja
Klasifikacija |
Kategorija 1 |
Kategorija 2 |
GHS piktogram opasnosti |
|
|
Reč upozorenja |
Opasnost |
Pažnja |
Obaveštenje o opasnosti |
H372: |
H373: |
Obaveštenja o merama |
P260 |
P260 |
Obaveštenja o merama predostrožnosti - reagovanje |
P314 |
P314 |
Obaveštenja o merama predostrožnosti - skladištenje |
|
|
Obaveštenja o merama predostrožnosti - odlaganje |
P501 |
P501 |
3.10.1. Definicije i opšta uputstva
3.10.1.1. Ovi kriterijumi se odnose na klasifikaciju supstanci ili smeša koje mogu predstavljati opasnost po zdravlje ljudi nakon aspiracije.
3.10.1.2. "Aspiracija" predstavlja unos supstance ili smeše u čvrstom ili tečnom stanju direktno kroz usta ili nosne otvore ili indirektno pri povraćanju, kada supstanca dospeva u dušnik i donje delove respiratornog sistema.
3.10.1.3. Toksičnost usled aspiracije uključuje ozbiljne akutne toksične efekte kao što su hemijska pneumonija, oštećenja pluća različitog stepena ili smrt nakon aspiracije.
3.10.1.4. Aspiracija započinje u trenutku udaha, a nastaje u toku vremena koje je potrebno za jedan udah, kada materijal uzročnik zastane na mestu gde se ukrštaju gornji deo respiratornog trakta i digestivni trakt i pređe u laringofaringealnu oblast.
3.10.1.5. Do aspiracije supstance ili smeše može doći i pri povraćanju, nakon gutanja. Ovo treba imati u vidu pri obeležavanju, naročito kada je zbog akutne toksičnosti preporučeno izazivanje povraćanja posle gutanja. Ako supstanca ili smeša predstavlja opasnost od toksičnosti usled aspiracije, preporuku o izazivanju povraćanja treba izmeniti.
3.10.1.6. Posebne napomene
3.10.1.6.1. Pregled medicinske literature o aspiraciji hemikalija otkriva da pojedini ugljovodonici (destilati nafte) i određeni hlorovani ugljovodonici predstavljaju opasnost po zdravlje ljudi usled aspiracije.
3.10.1.6.2. Kriterijumi za klasifikaciju zasnivaju se na kinematičkom viskozitetu. Sledeća formula omogućava pretvaranje dinamičkog u kinematički viskozitet:
dinamički viskozitet (mPa s) |
= kinematički viskozitet (mm2/s) |
gustina (g/cm3) |
Iako definicija aspiracije iz odeljka 3.10.1.2. ovog priloga obuhvata unos supstance ili smeše u čvrstom stanju u respiratorni sistem, klasifikacija za Kategoriju 1 u skladu sa tačkom (2) Tabele 3.10.1. koja je data u ovom prilogu primenjuje se samo na supstance ili smeše u tečnom stanju.
3.10.1.6.3. Klasifikacija aerosola/ magle(17)
Supstanca ili smeša u obliku aerosola i magle obično se pakuje u ambalažu kao što su posude pod pritiskom, posude sa raspršivačem sa okidačem i posude sa pumpicom. U ovim slučajevima, kriterijum za klasifikaciju na osnovu opasnosti od aspiracije jeste da li se u ustima može formirati količina supstance ili smeše koja bi zatim mogla biti aspirirana. Ako se supstanca ili smeša iz posude pod pritiskom raspršuje u vidu fine magle ili aerosola, nema mogućnosti da se u ustima formira količina koja bi mogla biti aspirirana. Međutim, ako se supstanca ili smeša iz posude pod pritiskom raspršuje u obliku mlaza, može doći do formiranja količine koja potom može biti aspirirana.
Obično je magla koja se izbacuje raspršivačem sa okidačem ili pumpicom gruba, pa može da formira količinu koja potom može biti aspirirana. Ukoliko se mehanizam za raspršivanje može skinuti sa pakovanja tako da sadržaj bude dostupan za gutanje, treba razmotriti klasifikaciju supstance ili smeše.
___________
(17) Magla je suspenzija finih kapljica tečnosti u gasu - kondezacioni i dispergovani aerosoli sa tečnom fazom
3.10.2. Kriterijumi za klasifikaciju supstanci
Tabela 3.10.1. Kriterijumi za opasnost od aspiracije
Kategorija opasnosti |
Kriterijumi |
Kategorija 1 |
Supstance koje su toksične za ljude ukoliko se aspiriraju ili za koje se smatra da predstavljaju opasnost od toksičnosti usled aspiracije. |
Napomena: Supstance iz kategorije 1 uključuju, između ostalih, ugljovodonike, terpentin i ulje iz borovih iglica.
3.10.3. Kriterijumi za klasifikaciju smeša
3.10.3.1. Klasifikacija smeše kada su dostupni podaci o svojstvima same smeše
Smeša se klasifikuje u kategoriju 1 na osnovu pouzdanih i kvalitetnih podataka iz iskustava na ljudima.
3.10.3.2. Klasifikacija smeše kada nisu dostupni podaci o svojstvima same smeše: Načela premošćavanja
3.10.3.2.1. Kada sama smeša nije ispitana radi utvrđivanja njene opasnosti od aspiracije, ali ima dovoljno podataka o pojedinačnim sastojcima i sličnim, već ispitanim smešama, da bi se odgovarajuće okarakterisala opasnost, ove podatke treba koristiti u skladu sa načelima premošćavanja datim u odeljku 1.1.3. ovog priloga.
U slučaju primene načela premošćavanja koja se odnose na razblaživanje, koncentracija sastojaka toksičnih usled aspiracije treba da bude 10% ili više.
3.10.3.3. Klasifikacija smeše kada su dostupni podaci za sve ili samo za neke njene sastojke
3.10.3.3.1. Kategorija 1
3.10.3.3.1.1. Smešu treba klasifikovati u kategoriju 1 ako sadrži ukupno 10% ili više supstance ili supstanci koje su klasifikovane u kategoriju 1 i ima kinematički viskozitet od 20,5 mm2/s ili manje, mereno na 40° C.
3.10.3.3.1.2. Smešu treba klasifikovati u kategoriju 1 i ako se ta smeša deli na dva ili više odvojenih slojeva, od kojih jedan sadrži 10% ili više supstance ili supstanci klasifikovanih u kategoriju 1 i ima kinematički viskozitet od 20,5 mm2/s ili manje, mereno na 40° C.
3.10.4. Elementi obeležavanja
Elementi obeležavanja za supstance i smeše koje ispunjavaju uslove da budu klasifikovane u ovu klasu opasnosti dati su u Tabeli 3.10.2. koja je data u ovom prilogu.
Tabela 3.10.2. Elementi obeležavanja za toksičnost usled aspiracije (opasnost od toksičnosti usled aspiracije)
Klasifikacija |
Kategorija 1 |
GHS piktogram opasnosti |
|
Reč upozorenja |
Opasnost |
Obaveštenje o opasnosti |
H304: |
Obaveštenja o merama predostrožnosti - prevencija |
|
Obaveštenja o merama predostrožnosti - reagovanje |
P301 + P310 |
Obaveštenja o merama predostrožnosti - skladištenje |
P405 |
Obaveštenja o merama predostrožnosti - odlaganje |
P501 |
OPASNOST PO ŽIVOTNU SREDINU
4.1. Opasnost po vodenu životnu sredinu
4.1.1. Definicije i opšta uputstva
4.1.1.1. Definicije
Akutna toksičnost po vodene organizme predstavlja svojstvo supstance da bude štetna po vodeni organizam koji je kratkotrajno izložen dejstvu te supstance.
Akutna (kratkotrajna) opasnost, za potrebe klasifikacije, predstavlja opasnost od supstance ili smeše usled njene akutne toksičnosti po organizam pri kratkotrajnoj izloženosti u vodenoj životnoj sredini.
Raspoloživost supstance predstavlja stepen rastvorljivosti ili stepen razdvajanja na sastavne delove. U slučaju metala, raspoloživost predstavlja stepen do kojeg se metalni jon nekog jedinjenja metala (M°) može odvojiti od ostatka molekula.
Bioraspoloživost (ili biološka raspoloživost) označava stepen u kom se supstanca resorbuje i raspodeljuje unutar organizma. Zavisi od fizičko-hemijskih osobina supstance, anatomije i fiziologije organizma, farmakokinetike i puta izlaganja. Raspoloživost neke supstance nije preduslov za njenu bioraspoloživost.
Bioakumulacija predstavlja zbirni rezultat unošenja, transformacije i eliminacije supstance iz organizma bilo kojim putem izlaganja (npr. vazduhom, vodom, sedimentom i hranom).
Biokoncentracija predstavlja zbirni rezultat unošenja, transformacije i eliminacije supstance iz organizma usled izloženosti u vodenoj sredini.
Hronična toksičnost po vodene organizme predstavlja svojstvo supstance da je štetna za vodene organizme koji su izloženi dejstvu te supstance i zavisi od faze životnog ciklusa tih organizama.
Razgradnja predstavlja razlaganje organskih molekula na manje molekule uz mogućnost potpune razgradnje na ugljen dioksid, vodu i soli.
ECx predstavlja efektivnu koncentraciju povezanu sa x% odgovora, odnosno koncentraciju pri kojoj se, u toku unapred definisanog vremena izlaganja, određeni efekat ispoljava kod x% populacije ispitivanog organizma.
Dugotrajna opasnost, za potrebe klasifikacije, predstavlja opasnost od supstance ili smeše usled njene hronične toksičnosti po organizam pri dugotrajnoj izloženosti u vodenoj životnoj sredini.
Koncentracija bez uočenog efekta (no observed effect concentration - NOEC, u daljem tekstu: NOEC) predstavlja ispitivanu koncentraciju odmah ispod najniže ispitane koncentracije sa statistički značajnim štetnim efektom. NOEC nema statistički značajan štetan efekat u poređenju sa kontrolnom grupom.
4.1.1.2. Osnovni pojmovi
4.1.1.2.0. Klasa opasnosti "Opasnost po vodenu životnu sredinu" obuhvata:
1) akutnu opasnost po vodenu životnu sredinu;
2) dugotrajnu opasnost po vodenu životnu sredinu.
4.1.1.2.1. Osnovni pojmovi koji se koriste pri klasifikaciji opasnosti po vodenu životnu sredinu su:
1) akutna toksičnost po vodene organizme;
2) hronična toksičnost po vodene organizme;
3) potencijal za bioakumulaciju ili stvarna bioakumulacija i
4) razgradnja (biotička ili abiotička) organskih hemikalija.
4.1.1.2.2. U postupku klasifikacije u odnosu na opasnost po vodenu životnu sredinu koriste se podaci dobijeni primenom metoda ispitivanja iz člana 8. stav 3. ovog pravilnika. U praksi se mogu koristiti i podaci dobijeni primenom drugih metoda koje su ekvivalentne metodama iz člana 8. ovog pravilnika pod uslovom da ove metode ispunjavaju uslove navedene u odeljku 1.1.0. ovog priloga.
Za potrebe klasifikacije uzimaju se podaci o toksičnosti dobijeni u ispitivanjima i na slatkovodnim i na morskim vrstama, pod uslovom da su metode ispitivanja ekvivalentne. Kada ovi podaci nisu dostupni, klasifikacija se zasniva na najboljim dostupnim podacima. Videti Deo 1. ovog priloga.
4.1.1.3. Druge napomene
4.1.1.3.1. Klasifikacija u odnosu na opasnost po životnu sredinu određuje se na osnovu opasnosti koju supstanca ili smeša predstavlja po vodenu životnu sredinu. Pod vodenom životnom sredinom podrazumevaju se vodeni organizmi i odgovarajući vodeni ekosistem. Osnov za utvrđivanje akutne (kratkotrajne) i dugotrajne opasnosti jeste toksičnost supstance ili smeše po vodene organizme, mada treba razmotriti i podatke o razgradnji i bioakumulaciji kada je potrebno.
4.1.2. Kriterijumi za klasifikaciju supstanci
4.1.2.1. Sistem za klasifikaciju prepoznaje opasnost po vodene organizme na osnovu obe, akutne i dugotrajne opasnosti supstance. Za dugotrajnu opasnost, definisane su posebne kategorije opasnosti zasnovane na gradaciji nivoa opasnosti. Najniže dostupne vrednosti toksičnosti između i u okviru različitih trofičkih nivoa (ribe, rakovi, alge/vodene biljke) koriste se za dodeljivanje odgovarajuće kategorije opasnosti. Postoje slučajevi kada je prikladno koristiti pristup utvrđivanja kvaliteta podataka.
4.1.2.2. Osnovni sistem klasifikacije supstanci sastoji se od jedne kategorije za akutnu opasnost i tri kategorije za dugotrajnu opasnost. Kategorije akutne i dugotrajne opasnosti primenjuju se nezavisno.
4.1.2.3. Kriterijumi za klasifikaciju supstanci u kategoriju Akutno 1 zasnivaju se samo na podacima o akutnoj toksičnosti po vodene organizme (EC50 ili LC50). Kriterijumi za klasifikaciju supstanci u jednu od kategorija Hronično 1 do 3 prate višestepeni pristup po kome se prvo utvrđuje da li se na osnovu dostupnih podataka o hroničnoj toksičnosti supstanca klasifikuje u dugotrajnu opasnost. Ako nema odgovarajućih podataka o hroničnoj toksičnosti, sledeći korak je kombinovanje dva tipa podataka, i to podataka o akutnoj toksičnosti po vodene organizme i podataka o sudbini u životnoj sredini (podaci o razgradnji i bioakumulaciji) (videti Sliku 4.1.1. koja je data u ovom prilogu).
Slika 4.1.1. Postupak klasifikacije supstanci u kategorije dugotrajne opasnosti po vodenu životnu sredinu
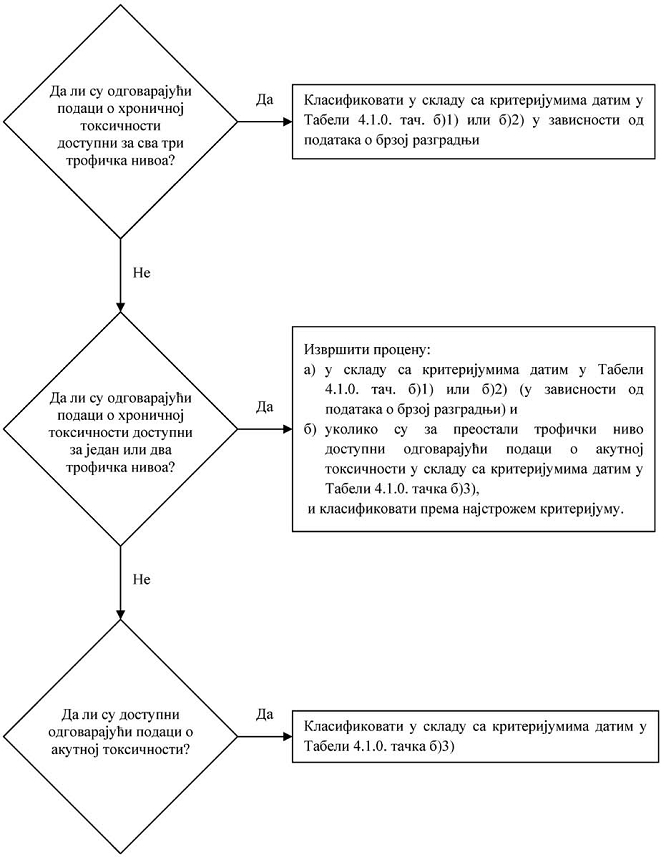
4.1.2.4. Sistem uvodi "sigurnosnu" klasifikaciju (kategorija Hronično 4) koja se koristi kada dostupni podaci ne omogućavaju klasifikaciju na osnovu propisanih kriterijuma u kategorije Akutno 1 ili Hronično 1 do 3, ali ima osnova za zabrinutost.
4.1.2.5. Supstance sa akutnom toksičnošću ispod 1 mg/l ili hroničnom toksičnošću ispod 0,1 mg/l (ako nisu brzo razgradljive) i 0,01 mg/l (ako su brzo razgradljive) kao sastojci smeše doprinose toksičnosti smeše čak i u malim koncentracijama i kada se primenjuje pristup sumiranja klasifikovanih sastojaka treba im dati veći značaj (videti Tabelu 4.1.0. Napomenu 1 i odeljak 4.1.3.5.5. ovog priloga).
4.1.2.6. Kriterijumi za klasifikaciju i kategorizaciju supstanci kao opasnih po vodenu životnu sredinu dati su u Tabeli 4.1.0.
Tabela 4.1.0. Kriterijumi za supstance opasne po vodenu životnu sredinu
a) |
Akutna (kratkotrajna) opasnost po vodenu životnu sredinu |
||
|
kategorija Akutno 1 (Napomena 1) |
||
|
96 h LC50 (za ribe) |
≤ 1 mg/l i/ili |
|
|
48 h EC50 (za rakove) |
≤ 1 mg/l i/ili |
|
|
72 ili 96 h ErC50 (za alge ili druge vodene biljke) |
≤ 1 mg/l (Napomena 2) |
|
b) |
Dugotrajna opasnost po vodenu životnu sredinu |
||
|
1) |
Supstance koje nisu brzo razgradljive (Napomena 3) i za koje su dostupni odgovarajući podaci o hroničnoj toksičnosti |
|
|
|
kategorija Hronično 1 (Napomena 1) |
|
|
|
hronična NOEC ili ECx (za ribe) |
≤ 0,1 mg/l i/ili |
|
|
hronična NOEC ili ECx (za rakove) |
≤ 0,1 mg/l i/ili |
|
|
hronična NOEC ili ECx (za alge ili druge vodene biljke) |
≤ 0,1 mg/l |
|
|
kategorija Hronično 2 |
|
|
|
hronična NOEC ili ECx (za ribe) |
> 0,1 do ≤ 1 mg/l i/ili |
|
|
hronična NOEC ili ECx (za rakove) |
> 0,1 do ≤ 1 mg/l i/ili |
|
|
hronična NOEC ili ECx (za alge ili druge vodene biljke) |
> 0,1 do ≤ 1 mg/l |
|
2) |
Brzo razgradljive supstance (Napomena 3) za koje su dostupni odgovarajući podaci o hroničnoj toksičnosti |
|
|
|
kategorija Hronično 1 (Napomena 1) |
|
|
|
hronična NOEC ili ECx (za ribe) |
≤ 0,01 mg/l i/ili |
|
|
hronična NOEC ili ECx (za rakove) |
≤ 0,01 mg/l i/ili |
|
|
hronična NOEC ili ECx (za alge ili druge vodene biljke) |
≤ 0,01 mg/l |
|
|
kategorija Hronično 2 |
|
|
|
hronična NOEC ili ECx (za ribe) |
> 0,01 do ≤ 0,1 mg/l i/ili |
|
|
hronična NOEC ili ECx (za rakove) |
> 0,01 do ≤ 0,1 mg/l i/ili |
|
|
hronična NOEC ili ECx (za alge ili druge vodene biljke) |
> 0,01 do ≤ 0,1 mg/l |
|
|
kategorija Hronično 3 |
|
|
|
hronična NOEC ili ECx (za ribe) |
> 0,1 do ≤ 1 mg/l i/ili |
|
|
hronična NOEC ili ECx (za rakove) |
> 0,1 do ≤ 1 mg/l i/ili |
|
|
hronična NOEC ili ECx (za alge ili druge vodene biljke) |
> 0,1 do ≤ 1 mg/l |
|
3) |
Supstance za koje nisu dostupni odgovarajući podaci o hroničnoj toksičnosti |
|
|
|
kategorija Hronično 1 (Napomena 1) |
|
|
|
96 h LC50 (za ribe) |
≤ 1 mg/l i/ili |
|
|
48 h EC50 (za rakove) |
≤ 1 mg/l i/ili |
|
|
72 ili 96 h ErC50 (za alge ili druge vodene biljke) |
≤ 1 mg/l (Napomena 2) |
|
|
i supstanca nije brzo razgradljiva i/ili je eksperimentalno određen BCF ≥ 500 (ili, u odsustvu BCF, log Kow ≥ 4) (Napomena 3) |
|
|
|
kategorija Hronično 2 |
|
|
|
96 h LC50 (za ribe) |
> 1 do ≤ 10 mg/l i/ili |
|
|
48 h EC50 (za rakove) |
> 1 do ≤ 10 mg/l i/ili |
|
|
72 ili 96 h ErC50 (za alge ili druge vodene biljke) |
> 1 do ≤ 10 mg/l (Napomena 2) |
|
|
i supstanca nije brzo razgradljiva i/ili je eksperimentalno određen BCF ≥ 500 (ili, u odsustvu BCF, log Kow ≥ 4) (Napomena 3) |
|
|
|
kategorija Hronično 3 |
|
|
|
96 h LC50 (za ribe) |
> 10 do ≤ 100 mg/l i/ili |
|
|
48 h EC50 (za rakove) |
> 10 do ≤ 100 mg/l i/ili |
|
|
72 ili 96 h ErC50 (za alge ili druge vodene biljke) |
> 10 do ≤ 100 mg/l (Napomena 2) |
|
|
i supstanca nije brzo razgradljiva i/ili je eksperimentalno određen BCF ≥ 500 (ili, u odsustvu BCF, log Kow ≥ 4) (Napomena 3) |
|
|
|
"Sigurnosna" klasifikacija |
|
|
|
kategorija Hronično 4 |
|
|
|
U slučajevima kada dostupni podaci nisu dovoljni za klasifikaciju prema navedenim kriterijumima, ali postoji sumnja da supstanca predstavlja opasnost po vodenu životnu sredinu, supstanca se klasifikuje u kategoriju Hronično 4. Na primer, slabo rastvorne supstance za koje nije uočena akutna toksičnost na nivou rastvorljivosti u vodi (Napomena 4), koje nisu brzo razgradljive u skladu sa odeljkom 4.1.2.9.5. ovog pravilnika i imaju eksperimentalno određen BCF ≥ 500 (ili, u odsustvu BCF, log Kow ≥ 4) što upućuje na potencijal bioakumulacije, klasifikuju se u ovu kategoriju, osim ako postoje drugi naučni dokazi koji ukazuju na to da supstancu ne treba klasifikovati, npr: vrednost NOEC za hroničnu toksičnost je veća od rastvorljivosti u vodi, odnosno veća od 1 mg/l, ili drugi dokazi o brzoj razgradnji u životnoj sredini pored onih koji su navedeni u odeljku 4.1.2.9.5. ovog pravilnika. |
|
Napomena 1: Ukoliko se supstanca klasifikuje u kategoriju Akutno 1 i/ili Hronično 1, neophodno je istovremeno navesti i odgovarajuće M-faktore (videti Tabelu 4.1.3. koja je data u ovom prilogu).
Napomena 2: Klasifikacija se zasniva na vrednosti ErC50 [= EC50 (stopa rasta)]. U slučajevima kada uslovi za utvrđivanje EC50 nisu jasno naznačeni ili nema podataka o ErC50, klasifikacija treba da se zasniva na najnižoj dostupnoj vrednosti EC50.
Napomena 3: Kada nisu dostupni upotrebljivi podaci o razgradnji, bilo da su podaci eksperimentalno određeni ili procenjeni, smatra se da supstanca nije brzo razgradljiva.
Napomena 4: "Nema akutne toksičnosti" označava da je vrednost L(E)C50 veća od rastvorljivosti u vodi. Koristi se i za slabo rastvorne supstance (rastvorljivost u vodi < 1 mg/l), kada postoje dokazi da ispitivanje akutne toksičnosti nije tačno merilo suštinske toksičnosti.
4.1.2.7. Toksičnost po vodene organizme
4.1.2.7.1. Akutna toksičnost po vodene organizme određuje se na osnovu vrednosti 96h LC50 za ribe, 48h EC50 za rakove, odnosno 72h ili 96h ErC50 za alge ili druge vodene biljke. Rezultati ispitivanja na ribama, rakovima i algama ili drugim vodenim biljkama, smatraju se reprezentativnim i za ostale taksonomske grupe i trofičke nivoe u vodenoj životnoj sredini. Podaci dobijeni na drugim organizmima (npr. Lemna spp.) uzimaju se u obzir ako je metodologija ispitivanja odgovarajuća. Ispitivanje inhibicije rasta algi spada u metode ispitivanja hronične toksičnosti, ali se vrednosti EC50 koriste i u postupku klasifikacije u slučaju akutne toksičnosti (vidi Napomenu 2).
4.1.2.7.2. Za određivanje hronične toksičnosti po vodene organizme u postupku klasifikacije koriste se podaci dobijeni metodama ispitivanja iz odeljka 4.1.1.2.2. ovog priloga, kao i rezultati dobijeni drugim potvrđenim i međunarodno priznatim metodama ispitivanja. Koriste se NOEC vrednosti ili druge vrednosti ekvivalentne ECx (npr. EC10).
4.1.2.8. Bioakumulacija
4.1.2.8.1. Usled bioakumulacije supstanci u vodenim organizmima može doći do pojave toksičnih efekata tokom dužeg vremenskog perioda čak i kada su stvarne koncentracije u vodi niske. Za organske supstance potencijal bioakumulacije određuje se pomoću koeficijenta raspodele oktanol/voda izraženog kao log Kow. Odnos između log Kow i biokoncentracije organske supstance izražava se pomoću faktora biokoncentracije (BCF) kod riba. Granična vrednost log Kow ≥ 4 koristi se za identifikaciju onih supstanci koje imaju stvarnu sposobnost biokoncentracije. Iako se na ovaj način može predstaviti potencijal bioakumulacije, bolje je koristiti eksperimentalno određen BCF ukoliko je dostupan. BCF ≥ 500 kod riba ukazuje na sposobnost biokoncentracije.
Uočava se povezanost hronične toksičnosti i potencijala bioakumulacije, s obzirom da toksičnost supstance zavisi od njene koncentracije u organizmu.
4.1.2.9. Brza razgradnja organskih supstanci
4.1.2.9.1. Brzo-razgradljive supstance se lako uklanjaju iz životne sredine. Iako se štetni efekti takvih supstanci mogu javiti, naročito u slučaju njihovog prosipanja ili hemijskog udesa, ovi efekti su lokalnog i kratkotrajnog karaktera. U odsustvu brze razgradnje u životnoj sredini toksičnost supstance u vodi može biti dugotrajna i dalekosežna.
4.1.2.9.2. Jedan od načina utvrđivanja brze razgradnje je korišćenje skrining testa biorazgradnje kojim se može utvrditi da je neka organska supstanca "lako biorazgradljiva". Ukoliko takvi podaci nisu dostupni, odnos BPK(5dana)/HPK ≥ 0,5 se smatra dobrim pokazateljem brze razgradnje supstance. Smatra se da supstanca verovatno nije perzistentna ukoliko se skrining testom utvrdi da je ta supstanca brzo razgradljiva u vodenoj životnoj sredini. Ukoliko se u skrining testu dobije negativan rezultat to se ne uzima kao dokaz da se supstanca ne razlaže brzo u životnoj sredini, već se razmatraju i drugi dokazi o brzoj razgradnji supstance u životnoj sredini, a naročito kada supstanca deluje inhibitorno na mikrobiološku aktivnost pri koncentracijama koje se koriste u metodama ispitivanja. Uvode se i dodatni kriterijumi za klasifikaciju koji omogućavaju korišćenje podataka koji pokazuju da se više od 70% supstance biotički ili abiotički razgradi u vodenoj sredini tokom 28 dana. Ukoliko se razgradnja supstance dokaže u uslovima koji odgovaraju stvarnim uslovima životne sredine onda je ispunjen kriterijum brze razgradljivosti.
4.1.2.9.3. Podaci o razgradnji supstanci dostupni u obliku poluvremena razgradnje mogu se koristiti za određivanje brze razgradnje, pod uslovom da je postignuta potpuna biorazgradnja supstance, tj. potpuna mineralizacija. Primarna biorazgradljivost može se koristiti za procenu brze razgradljivosti samo ako se proizvodi razgradnje ne mogu klasifikovati kao opasni po vodenu životnu sredinu.
4.1.2.9.4. Gore navedeni kriterijumi za klasifikaciju proizilaze iz činjenice da razgradnja u životnoj sredini može biti biotička i abiotička. Hidroliza se može uzeti u obzir samo ako se proizvodi hidrolize ne mogu klasifikovati kao opasni po vodenu životnu sredinu.
4.1.2.9.5. Supstance su brzo razgradljive ako je zadovoljen jedan od sledećih kriterijuma:
1) ako se u 28-dnevnom ispitivanju biorazgradljivosti postigne najmanje sledeći nivo razgradnje:
- 70% u ispitivanjima koja se zasnivaju na rastvorenom organskom ugljeniku,
- 60% od teoretskog maksimuma, u ispitivanjima koji se zasnivaju na potrošnji kiseonika ili na stvaranju ugljendioksida.
Ovi nivoi biorazgradnje postižu se u periodu od deset dana od početka razgradnje, a za početak se uzima vreme kada se razgradilo 10% supstance osim ako je supstanca identifikovana kao supstanca nepoznatog ili promenljivog sastava, složeni proizvodi reakcije ili biološki materijali (Unknown or Variable Composition, Complex reaction products or Biological materials - UVCB) ili kao složena, multikonstituentna supstanca sa strukturno sličnim sastojcima. U ovom slučaju i kada je dovoljno opravdano, uzima se da se nivoi razgradnje umesto u okviru 10-dnevnog perioda mogu postići za 28 dana; ili
2) u slučajevima kada su dostupni samo podaci o hemijskoj potrošnji kiseonika (HPK) i biološkoj potrošnji kiseonika za 5 dana (BPK5), ako je BPK5/HPK ≥ 0,5 ili
3) ako postoje drugi naučni dokazi da se više od 70% supstance može razgraditi (biotički i/ili abiotički) u vodenoj životnoj sredini tokom perioda od 28 dana.
4.1.2.10. Neorganska jedinjenja i metali
4.1.2.10.1. Koncept razgradnje koji se primenjuje na organske materije ima ograničen značaj ili nema značaja za neorganska jedinjenja i metale. Neorganska jedinjenja i metali se uobičajenim procesima u životnoj sredini mogu transformisati tako da se ili poveća ili smanji bioraspoloživost toksičnih oblika supstance. Podaci o bioakumulaciji oprezno se koriste prilikom klasifikacije neorganskih jedinjenja i metala.
4.1.2.10.2. Slabo rastvorna neorganska jedinjenja i metali mogu biti akutno ili hronično toksični u vodenoj životnoj sredini u zavisnosti od toksičnosti bioraspoloživih oblika neorganske supstance i brzine rastvaranja i količine neorganskog oblika supstance koji je prešao u rastvor. Prilikom donošenja odluke o klasifikaciji utvrđuje se kvalitet svih podataka.
4.1.3. Kriterijumi za klasifikaciju smeša
4.1.3.1. Sistem klasifikacije za smeše obuhvata sve kategorije opasnosti koje se koriste za supstance, tj. kategorije Akutno 1 i Hronično 1 do 4. U postupku klasifikacije smeše u odnosu na opasnost po vodenu životnu sredinu, uzimaju se u obzir svi dostupni podaci o tzv. značajnim sastojcima smeše.
Značajni sastojci smeše su:
- sastojci koji su klasifikovani u Akutno 1 ili Hronično 1, a koji su u smeši prisutni u koncentraciji od 0,1% (m/m) ili većoj ili
- sastojci koji su klasifikovani u Hronično 2, 3 i 4, a koji su u smeši prisutni u koncentraciji od 1% (m/m) ili većoj.
U određenim slučajevima (npr. smeša sa veoma toksičnim sastojcima (videti odeljak 4.1.3.5.5.5 ovog priloga)), i sastojak smeše prisutan u nižim koncentracijama od gore navedenih može se uzeti u obzir kao značajan sastojak za klasifikaciju smeše u odnosu na opasnost po vodenu životnu sredinu. Supstance koje su klasifikovane u Akutno 1 ili Hronično 1, treba uzeti u obzir ako je njihova koncentracija (0,1/M)% ili veća (za objašnjenje M faktora videti odeljak 4.1.3.5.5.5. ovog priloga).
4.1.3.2. U postupku klasifikacije smeše u odnosu na opasnost po vodenu životnu sredinu koristi se višestepeni pristup koji zavisi od vrste podataka za svaku smešu i njene sastojke. Šematski prikaz procedura koje treba primeniti dat je na slici 4.1.2. koja je data u ovom prilogu.
Višestepeni pristup uključuje:
- klasifikaciju na osnovu ispitanih smeša;
- klasifikaciju na osnovu načela premošćavanja;
- korišćenje "metode sumiranja klasifikovanih sastojaka" i/ili "formule aditivnosti".
Slika 4.1.2. Višestepeni pristup klasifikaciji smeša u odnosu na akutnu i dugotrajnu opasnost po vodenu životnu sredinu
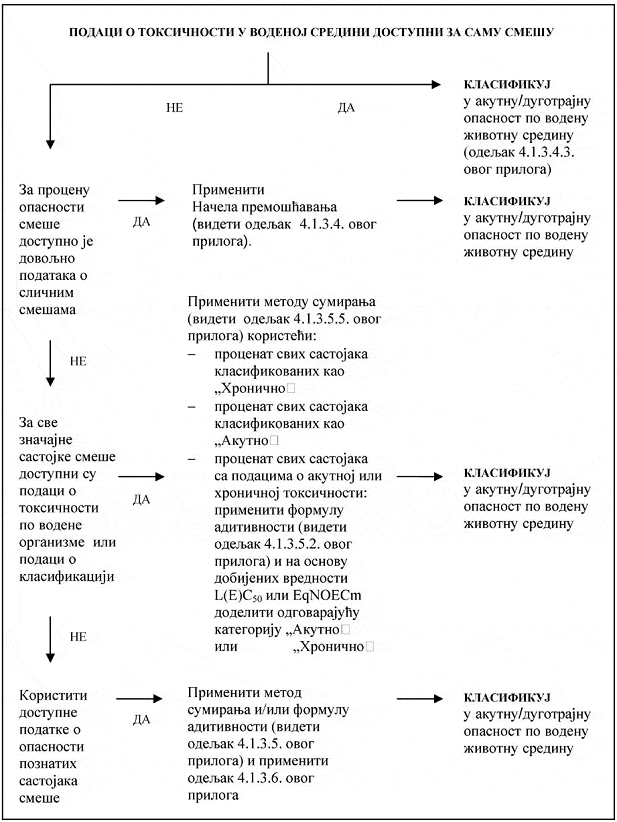
4.1.3.3. Klasifikacija smeša kada su podaci o toksičnosti dostupni za smešu u celini
4.1.3.3.1. Kada je smeša ispitana radi određivanja njene toksičnosti po vodene organizme, klasifikacija se vrši na osnovu rezultata ispitivanja prema kriterijumima koji važe za supstance. Klasifikacija se obično zasniva na podacima dobijenim u ispitivanjima na ribama, rakovima i algama, odnosno vodenim biljkama (videti odeljke 4.1.2.7.1. i 4.1.2.7.2. ovog priloga). Kada nedostaju odgovarajući podaci o akutnoj ili hroničnoj toksičnosti same smeše, primenjuju se načela premošćavanja ili metoda sumiranja (videti odeljke 4.1.3.4. i 4.1.3.5. ovog priloga).
4.1.3.3.2. Klasifikacija smeše u odnosu na dugotrajnu opasnost zahteva dodatne podatke o razgradljivosti i, u određenim slučajevima, bioakumulaciji. Ne vrše se ispitivanja razgradljivosti i bioakumulacije smeše, jer ih je teško tumačiti, tj. ova ispitivanja mogu biti značajna samo za pojedinačne supstance.
4.1.3.3.3. Klasifikacija smeše u kategoriju Akutno 1
a) Kada su dostupni odgovarajući podaci o akutnoj toksičnosti (L(E)C50 ili EC50) dobijeni ispitivanjem smeše u celini i kada ti podaci pokazuju da je L(E)C50 ≤ 1 mg/l, smeša se klasifikuje u kategoriju Akutno 1, u skladu sa Tabelom 4.1.0. tačka a).
b) Kada su dostupni podaci o akutnoj toksičnosti (vrednost(i) LC50 ili EC50) dobijeni ispitivanjem smeše u celini i kada ti podaci pokazuju da je vrednost L(E)C50 > 1 mg/l za sve trofičke nivoe, nema potrebe da se smeša klasifikuje u odnosu na akutnu opasnost.
4.1.3.3.4. Klasifikacija u kategorije Hronično 1, 2 i 3
a) Kada su dostupni odgovarajući podaci o hroničnoj toksičnosti (ECx ili NOEC) dobijeni ispitivanjem smeše u celini i kada ti podaci pokazuju da je ECx ili NOEC ispitane smeše ≤ 1 mg/l:
1) smeša se klasifikuje u kategoriju Hronično 1, 2 ili 3 u skladu sa Tabelom 4.1.0. tačka b) 2) kao brzo razgradljiva, ako se na osnovu dostupnih podataka može zaključiti da su svi značajni sastojci smeše brzo razgradljivi;
2) smeša se klasifikuje u kategoriju Hronično 1 ili 2 u svim drugim slučajevima, u skladu sa Tabelom 4.1.0. tačka b) 1) kao smeša koja nije brzo razgradljiva;
b) Kada su dostupni odgovarajući podaci o hroničnoj toksičnosti (ECx ili NOEC) dobijeni ispitivanjem smeše u celini i kada ti podaci pokazuju da je ECx ili NOEC ispitane smeše > 1 mg/l za sve trofičke nivoe, nema potrebe da se smeša klasifikuje u odnosu na dugotrajnu opasnost u kategorije Hronično 1, 2 ili 3.
4.1.3.3.5. Klasifikacija smeše u kategoriju Hronično 4
Ako postoje razlozi za zabrinutost, smeša se klasifikuje u kategoriju Hronično 4 ("sigurnosna" klasifikacija) u skladu sa Tabelom 4.1.0. ovog priloga.
4.1.3.4. Klasifikacija smeša kada podaci o toksičnosti smeše u celini nisu dostupni: Načela premošćavanja
4.1.3.4.1. Kada sama smeša nije ispitana u odnosu na opasnosti po vodenu životnu sredinu, ali postoji dovoljno podataka o pojedinačnim sastojcima i sličnim ispitanim smešama, ovi podaci se koriste u postupku klasifikacije u skladu sa načelima premošćavanja datim u odeljku 1.1.3. ovog priloga. U slučaju primene načela premošćavanja za razblaživanje postupa se u skladu sa odeljcima 4.1.3.4.2. i 4.1.3.4.3. ovog priloga.
4.1.3.4.2. Razblaživanje: Ukoliko je smeša dobijena razblaživanjem neke druge ispitane smeše ili supstance, klasifikovane u odnosu na opasnost po vodenu životnu sredinu, rastvaračem koji je klasifikovan u istu ili nižu kategoriju opasnosti u odnosu na najmanje toksičan početni sastojak smeše i za koji se ne očekuje da utiče na stepen opasnosti ostalih sastojaka, tada se smeša dobijena razblaživanjem može klasifikovati isto kao i originalna ispitana smeša ili supstanca. Alternativno, može se primeniti metoda objašnjena u odeljku 4.1.3.5. ovog priloga.
4.1.3.4.3. Ukoliko se smeša dobija razblaživanjem druge klasifikovane smeše ili supstance vodom ili nekom drugom netoksičnom hemikalijom, toksičnost smeše može se izračunati na osnovu podataka o originalnoj smeši ili supstanci.
4.1.3.5. Klasifikacija smeša kada su podaci o toksičnosti dostupni za pojedine ili za sve sastojke smeše
4.1.3.5.1. Klasifikacija smeše zasniva se na sumiranju koncentracija njenih klasifikovanih sastojaka. Procenat sastojaka klasifikovanih u "Akutno" ili "Hronično" primenjuje se direktno u metodi sumiranja. Primena ove metode detaljno je objašnjena u odeljku 4.1.3.5.5. ovog priloga.
4.1.3.5.2. Smeše se mogu sastojati od kombinacije sastojaka koji su klasifikovani (kao Akutno 1 i/ili Hronično 1, 2, 3 ili 4) i drugih za koje su dostupni odgovarajući podaci o toksičnosti dobijeni ispitivanjima. Kada su odgovarajući podaci o toksičnosti dostupni za više od jednog sastojka smeše, kombinovana toksičnost tih sastojaka izračunava se pomoću formula aditivnosti datih u ovom odeljku pod tač. a) ili b), u zavisnosti od prirode dostupnih podataka:
a) na osnovu akutne toksičnosti po vodenu životnu sredinu:
![]()
pri čemu je:
Ci - koncentracija i-tog sastojka (maseni procenat);
L(E)C50i - LC50 ili EC50 za sastojak i u mg/l;
h - broj sastojaka, ide od 1 do n;
L(E)C50m - LC50 ili EC50 dela smeše za koji su dostupni podaci dobijeni ispitivanjima.
Izračunata toksičnost može se iskoristiti da se ovom delu smeše dodeli kategorija akutne opasnosti, koja se zatim koristi prilikom primene metode sumiranja;
b) na osnovu hronične toksičnosti po vodenu životnu sredinu:
![]()
pri čemu je:
Ci - koncentracija i-tog sastojka (maseni procenat) koja obuhvata brzo razgradljive sastojke;
Cj - koncentracija j-tog sastojka (maseni procenat) koja obuhvata sastojke koji nisu brzo razgradljivi;
NOECi - NOEC (ili druge priznate mere za hroničnu toksičnost) za sastojak i koja obuhvata brzo razgradljive sastojke, u mg/l;
NOECj - NOEC (ili druge priznate mere za hroničnu toksičnost) za sastojak j koja obuhvata sastojke koji nisu brzo razgradljivi, u mg/l;
n - broj sastojaka, i i j idu od 1 do n;
EqNOECm - ekvivalentna NOEC dela smeše za koji su dostupni podaci dobijeni ispitivanjima.
Ekvivalentna toksičnost odražava činjenicu da su supstance koje nisu brzo razgradljive klasifikovane u kategoriju opasnosti koja je za jedan nivo viša u odnosu na klasifikaciju brzo razgradljivih supstanci.
Izračunata ekvivalentna toksičnost može se iskoristiti da se ovom delu smeše dodeli, kategorija dugotrajne opasnosti, u skladu sa kriterijumima za brzo razgradljive supstance (videti Tabelu 4.1.0. tačka b) 2)), koja se zatim koristi prilikom primene metode sumiranja
4.1.3.5.3. Kada se primenjuje formula aditivnosti za deo smeše, toksičnost tog dela smeše izračunava se korišćenjem, za svaku supstancu, vrednosti toksičnosti koje se odnose na istu taksonomsku grupu (tj. ribe, rakove, alge ili ekvivalentnu), a zatim se koristi najviša dobijena toksičnost (najniža koncetracija), tj. koristi se najosetljivija od tri taksonomske grupe. U slučaju da podaci o toksičnosti nisu dostupni za sve sastojke u okviru iste taksonomske grupe, vrednost toksičnosti svakog od sastojaka koja se koristi bira se na isti način na koji se vrednosti toksičnosti biraju radi klasifikacije supstanci, tj. koristi se viša toksičnost (dobijena za najosetljiviji ispitivani organizam). Izračunata akutna i hronična toksičnost se zatim koriste radi procene da li će ovaj deo smeše biti klasifikovan kao Akutno 1 i/ili Hronično 1, 2 ili 3, primenom istih kriterijuma propisanih za supstance.
4.1.3.5.4. Ukoliko je smeša klasifikovana na više od jednog načina, koristiti se onaj način koji daje najstrožiji rezultat.
4.1.3.5.5. Metoda sumiranja
4.1.3.5.5.1. Obrazloženje
4.1.3.5.5.1.1. U slučaju klasifikacionih kategorija za supstance Hronično 1, 2 i 3, osnovni kriterijumi toksičnosti razlikuju se pri prelasku iz jedne kategorije opasnosti u drugu za faktor 10. Supstance klasifikovane na osnovu visoke vrednosti LC50 ili EC50 doprinose klasifikaciji smeše u nižu kategoriju opasnosti. Prilikom izračunavanja ovih klasifikacionih kategorija zajedno se razmatra doprinos svih supstanci klasifikovanih u Hronično 1, 2 ili 3.
4.1.3.5.5.1.2. Kada smeša sadrži sastojke klasifikovane u kategoriju Akutno 1 ili Hronično 1, čija je akutna toksičnost ispod 1 mg/l i/ili hronična toksičnost ispod 0,1 mg/l (ako nisu brzo razgradljivi) i 0,01 mg/l (ako jesu brzo razgradljivi), ovi sastojci doprinose toksičnosti smeše čak i u niskim koncentracijama. Aktivne supstance u pesticidima često imaju visoku toksičnost po vodene organizme, kao i neke druge supstance, npr. organometalna jedinjenja. U takvim slučajevima primena opštih graničnih koncentracija dovodi do neodgovarajuće, odnosno podcenjene klasifikacije smeše. Zbog toga se koriste M faktori za visoko toksične sastojke, kao što je dato u odeljku 4.1.3.5.5.5. ovog priloga.
4.1.3.5.5.2. Postupak klasifikacije
4.1.3.5.5.2.1. Klasifikacija smeše u višu kategoriju opasnosti nadjačava klasifikaciju u nižu kategoriju opasnosti, npr. klasifikacija u Hronično 1 nadjačava klasifikaciju u Hronično 2. Postupak klasifikacije je završen ako je kao rezultat klasifikacije dobijena kategorija Hronično 1. Hronično 1 je najviša moguća kategorija opasnosti, zato nije potrebno nastaviti sa daljim postupkom klasifikacije.
4.1.3.5.5.3. Klasifikacija u kategoriju Akutno 1
4.1.3.5.5.3.1. Prvo se razmatraju svi sastojci klasifikovani u kategoriju Akutno 1. Ukoliko je suma procentualnih koncentracija ovih sastojaka pomnoženih njihovim odgovarajućim M-faktorima veća od 25% smeša se klasifikuje u kategoriju Akutno 1.
4.1.3.5.5.3.2. Klasifikacija smeša na osnovu akutne opasnosti primenom metode sumiranja klasifikovanih sastojaka data je u Tabeli 4.1.1. koja je data u ovom prilogu.
Tabela 4.1.1. Klasifikacija smeše u odnosu na akutnu opasnost po vodenu životnu sredinu primenom metode sumiranja koncentracija klasifikovanih sastojaka smeše
Suma sastojaka klasifikovanih kao |
Smeša je klasifikovana kao |
Kategorija 1, akutno x M ≥ 25% |
Akutno 1 |
Napomena: Za objašnjenje M-faktora videti odeljak 4.1.3.5.5.5. ovog priloga.
4.1.3.5.5.4. Klasifikacija u kategorije Hronično 1, 2, 3 i 4
4.1.3.5.5.4.1. Prvo se razmatraju svi sastojci klasifikovani u kategoriju Hronično 1. Ukoliko je zbir procentualnih koncentracija ovih sastojaka pomnoženih njihovim odgovarajućim M-faktorima jednak ili veći od 25% smeša se klasifikuje u kategoriju Hronično 1. Ukoliko je rezultat izračunavanja klasifikacija smeše u kategoriju Hronično 1, postupak klasifikacije je završen.
4.1.3.5.5.4.2. U slučajevima kada smeša nije klasifikovana u kategoriju Hronično 1, razmatra se klasifikacija smeše u kategoriju Hronično 2. Smeša se klasifikuje u kategoriju Hronično 2, ukoliko je zbir procentualnih koncentracija svih sastojaka klasifikovanih u kategoriju Hronično 1, pomnoženih njihovim odgovarajućim M-faktorima pomnožen brojem 10, sabran sa zbirom procentualnih koncentracija svih sastojaka koji su klasifikovani u kategoriju Hronično 2, jednak ili veći od 25%. Ukoliko je rezultat izračunavanja klasifikacija smeše u kategoriju Hronično 2, postupak klasifikacije je završen.
4.1.3.5.5.4.3. U slučajevima kada smeša nije klasifikovana ni u kategoriju Hronično 1, ni u kategoriju Hronično 2, razmatra se njena klasifikacija u kategoriju Hronično 3. Smeša se klasifikuje u kategoriju Hronično 3, ukoliko je zbir procentualnih koncentracija svih sastojaka klasifikovanih u kategoriju Hronično 1, pomnoženih njihovim odgovarajućim M-faktorima, pomnožen brojem 100, sabran, sa zbirom procentualnih koncentracija sastojaka klasifikovanih u kategoriju Hronično 2 pomnoženim sa brojem 10 i sabran sa zbirom procentualnih koncentracija sastojaka klasifikovanih u kategoriju Hronično 3, jednak ili veći od 25%.
4.1.3.5.5.4.4. U slučaju kada smeša nije klasifikovana u kategoriju Hronično 1, 2 ili 3, razmatra se klasifikacija u kategoriju Hronično 4. Smeša se klasifikuje u kategoriju Hronično 4, ukoliko je zbir procentualnih koncentracija svih sastojaka klasifikovanih u kategoriju Hronično 1, 2, 3 i 4, jednak ili veći od 25%.
4.1.3.5.5.4.5. Klasifikacija smeša na osnovu dugotrajne opasnosti, primenom metode sumiranja klasifikovanih sastojaka data je u Tabeli 4.1.2. koja je data u ovom prilogu.
Tabela 4.1.2. Klasifikacija smeše u odnosu na dugotrajnu opasnost po vodenu životnu sredinu primenom metode sumiranja koncentracija klasifikovanih sastojaka
Suma sastojaka klasifikovanih kao |
Smeša se klasifikuje kao |
Hronično 1 x M(*) ≥ 25% |
Hronično 1 |
(M x 10 x Hronično 1) + Hronično 2 ≥ 25% |
Hronično 2 |
(M x 100 x Hronično 1) + (10 x Hronično 2) + Hronično 3 ≥ 25% |
Hronično 3 |
Hronično 1 + Hronično 2 + Hronično 3 + Hronično 4 ≥ 25% |
Hronično 4 |
Napomena(*): Za objašnjenje M-faktora videti odeljak 4.1.3.5.5.5. ovog priloga. |
|
4.1.3.5.5.5. Smeše sa visoko toksičnim sastojcima
4.1.3.5.5.5.1. Sastojci klasifikovani u kategoriju Akutno 1 i kategoriju Hronično 1, sa toksičnošću ispod 1 mg/l i/ili hroničnom toksičnošću ispod 0,1 mg/l (ako nisu brzo razgradljive) i 0,01 mg/l (ako su brzo razgradljive) doprinose toksičnosti smeše čak i u niskoj koncentraciji i daje im se veći značaj pri primeni metode sumiranja klasifikacija. Kada smeša sadrži sastojke klasifikovane u kategoriju Akutno 1 ili kategoriju Hronično 1, primenjuje se jedno od sledećeg:
- višestepeni pristup opisan u odeljcima 4.1.3.5.5.3 i 4.1.3.5.5.4 ovog priloga, tako što se sabiraju koncentracije sastojaka klasifikovanih u kategoriju Akutno 1 i kategoriju Hronično 1 pomnožene faktorom, umesto prostog sabiranja procenata. Ovo znači da se koncentracija sastojaka klasifikovanih u kategoriju Akutno 1, iz leve kolone Tabele 4.1.1. i koncentracija sastojaka klasifikovanih u kategoriju Hronično 1 iz leve kolone Tabele 4.1.2. množe odgovarajućim M-faktorom. M-faktori za ove sastojke se određuju na osnovu vrednosti LC50 ili EC50, kao što je dato u Tabeli 4.1.3. koja je data u ovom prilogu. U postupku klasifikacije smeša koje sadrže sastojke klasifikovane u kategoriju Akutno 1, ili kategoriju Hronično 1 moraju biti poznate vrednosti M-faktora da bi se primenila metoda sumiranja;
- formula aditivnosti (videti odeljak 4.1.3.5.2. ovog priloga), pod uslovom da su podaci o toksičnosti dostupni za sve visoko toksične sastojke smeše i da postoje pouzdani dokazi da svi drugi sastojci, uključujući i one za koje podaci o specifičnoj akutnoj i/ili hroničnoj toksičnosti nisu dostupni, imaju nižu toksičnost ili uopšte nisu toksični i ne doprinose opasnosti smeše po životnu sredinu.
Tabela 4.1.3. M-faktori za visoko toksične sastojke smeše
Akutna toksičnost |
M-faktor |
Hronična toksičnost |
M-faktor |
|
L(E)C50 vrednost u mg/l |
|
NOEC vrednost u mg/l |
NRD(1) sastojci |
RD(2) sastojci |
0,1 < L(E)C50 ≤ 1 |
1 |
0,01 < NOEC ≤ 0,1 |
1 |
- |
0,01 < L(E)C50 ≤ 0,1 |
10 |
0,001 < NOEC ≤ 0,01 |
10 |
1 |
0,001 < L(E)C50 ≤ 0,01 |
100 |
0,0001 < NOEC ≤ 0,001 |
100 |
10 |
0,0001 < L(E)C50 ≤ 0,001 |
1000 |
0,00001 < NOEC ≤ 0,0001 |
1000 |
100 |
0,00001 L(E)C50 ≤ 0,0001 |
10000 |
0,000001 < NOEC ≤ 0,00001 |
10000 |
1000 |
(progresija se nastavlja za faktor 10) |
(progresija se nastavlja za faktor 10) |
|||
(1) nije brzo razgradljivo (non-rapidly degradable - NRD) |
||||
4.1.3.6. Klasifikacija smeša sa sastojcima o kojima nema podataka koji se mogu upotrebiti u postupku klasifikacije:
4.1.3.6.1. U slučaju da ne postoje podaci o akutnoj i/ili dugotrajnoj opasnosti po vodenu životnu sredinu za jedan ili više značajnih sastojaka, smeša se ne može sa sigurnošću klasifikovati u jednu ili više kategorija opasnosti. U tom slučaju smeša se klasifikuje samo na osnovu poznatih sastojaka, i dodaje se obaveštenje na etiketi i u bezbednosnom listu: "Sadrži x% sastojaka nepoznate opasnosti po vodenu životnu sredinu."
4.1.4. Elementi obeležavanja
Elementi obeležavanja za supstance i smeše koje ispunjavaju uslove da budu klasifikovane u ovu klasu opasnosti dati su u Tabeli 4.1.4. koja je data u ovom prilogu.
Tabela 4.1.4. Elementi obeležavanja za opasnost po vodenu životnu sredinu
AKUTNA OPASNOST PO VODENU ŽIVOTNU SREDINU |
|
|
Akutno 1 |
GHS piktogram opasnosti |
|
Reč upozorenja |
Pažnja |
Obaveštenje o opasnosti |
H400: |
Obaveštenja o merama predostrožnosti - prevencija |
P273 |
Obaveštenja o merama predostrožnosti - reagovanje |
P391 |
Obaveštenja o merama predostrožnosti - skladištenje |
|
Obaveštenja o merama predostrožnosti - odlaganje |
P501 |
DUGOTRANJA OPASNOST PO VODENU ŽIVOTNU SREDINU |
||||
|
Hronično 1 |
Hronično 2 |
Hronično 3 |
Hronično 4 |
GHS piktogram opasnosti |
|
|
Ne koristi se GHS piktogram opasnosti |
Ne koristi se GHS piktogram opasnosti |
Reč upozorenja |
Pažnja |
Nema reči upozorenja |
Nema reči upozorenja |
Nema reči upozorenja |
Obaveštenje o opasnosti |
H410: |
H411: |
H412: |
H413: |
Obaveštenja o merama predostrožnosti - prevencija |
P273 |
P273 |
P273 |
P273 |
Obaveštenja o merama predostrožnosti - reagovanje |
P391 |
P391 |
|
|
Obaveštenja o merama predostrožnosti - skladištenje |
|
|
|
|
Obaveštenja o merama predostrožnosti - odlaganje |
P501 |
P501 |
P501 |
P501 |
DODATNE OPASNOSTI
5.1. Opasnost po ozonski omotač
5.1.1. Definicije i opšta uputstva
5.1.1.1. Potencijal oštećenja ozonskog omotača (ODP) je integrativna veličina, različita za svaku vrstu izvora halogenovanih ugljovodonika, koja predstavlja očekivani stepen oštećenja ozona u stratosferi od strane određenog halogenovanog ugljovodonika u odnosu na istu masu trihlorofluorometana (CFC-11). Po zvaničnoj definiciji, ODP jeste odnos integrisanog poremećaja ukupnog ozona za diferencijalne masene emisije određenog jedinjenja i jednake emisije CFC-11.
5.1.1.2. Supstanca opasna po ozonski omotač jeste supstanca koja na osnovu raspoloživih dokaza o njenim svojstvima i pretpostavljenoj ili uočenoj sudbini i ponašanju u životnoj sredini može predstavljati opasnost po strukturu i/ili funkcionisanje ozonskog omotača u stratosferi. Ovo uključuje supstance koje su navedene u propisima kojima se uređuju supstance koje oštećuju ozonski omotač.
5.1.2. Kriterijumi za klasifikaciju supstanci
Supstanca se klasifikuje kao opasna po ozonski omotač (Kategorija 1) kada dostupni podaci o svojstvima supstance i pretpostavljenoj ili uočenoj sudbini i ponašanju u životnoj sredini ukazuju da supstanca može predstavljati opasnost po strukturu, odnosno ulogu ozonskog omotača u stratosferi.
5.1.3. Kriterijumi za klasifikaciju smeša
Smeša se klasifikuje kao opasna po ozonski omotač (Kategorija 1) na osnovu pojedinačnih koncentracija supstanci koje ulaze u sastav smeše, a koje su klasifikovane kao opasne po ozonski omotač i u skladu sa Tabelom 5.1. koja je data u ovom prilogu.
Tabela 5.1. Opšte granične koncentracije za supstance (u smeši) klasifikovane kao opasne po ozonski omotač (Kategorija 1), koje impliciraju klasifikaciju smeše kao opasne po ozonski omotač
Klasifikacija supstance |
Klasifikacija smeše |
Opasno po ozonski omotač (Kategorija 1) |
C 3 0,1% |
5.1.4. Elementi obeležavanja
Elementi obeležavanja za supstance i smeše koje ispunjavaju uslove da budu klasifikovane u ovu klasu opasnosti dati su u Tabeli 5.2. koja je data u ovom prilogu.
Tabela 5.2. Elementi obeležavanja za opasnost po ozonski omotač
GHS piktogram opasnosti |
|
Reč upozorenja |
Pažnja |
Obaveštenje o opasnosti |
H420: Šteti javnom zdravlju i životnoj sredini tako što oštećuje ozon u gornjoj atmosferi |
Obaveštenja o merama predostrožnosti |
P502 |